DANH SÁCH CÁC QUY TRÌNH KỸ THUẬT CHUYÊN NGÀNH VI SINH HỌC
(Ban hành kèm theo Quyết định số: 26/QĐ-BYT ngày 03 tháng 01 năm 2014 của Bộ trưởng Bộ Y tế)
| TT | TÊN QUY TRÌNH KỸ THUẬT | |||
| Danh mục xét nghiệm vi khuẩn | ||||
| A. Vi khuẩn chung | ||||
| 1 | Vi khuẩn nhuộm soi | |||
| 2 | Vi khuẩn test nhanh | |||
| B. Mycobacteria | ||||
| 17 | AFB trực tiếp nhuộm Ziehl-Neelsen | |||
| 18 | AFB trực tiếp nhuộm huỳnh quang | |||
| 21 | Mycobacterium tuberculosis Mantoux | |||
| 38 | Mycobacterium leprae nhuộm soi | |||
| C. Vibrio cholerae | ||||
| 41 | Vibrio cholerae nhuộm soi | |||
| 42 | Vibrio cholerae nhuộm huỳnh quang | |||
| F. Các vi khuẩn khác | ||||
| 54 | Chlamydia test nhanh | |||
| 55 | Chlamydia nhuộm huỳnh quang | |||
| Danh mục xét nghiệm virus | ||||
| A. Virus chung | ||||
| 74 | Virus test nhanh | |||
| B. Hepatitis virus | ||||
| 77 | HBsAg test nhanh | |||
| C. HIV | ||||
| 117 | HIV Ab test nhanh | |||
| D. Dengue virus | ||||
| 127 | Dengue virus NS1Ag test nhanh | |||
| 128 | Dengue virus NS1Ag/IgM/IgG test nhanh | |||
| 129 | Dengue virus IgM/IgG test nhanh | |||
| F. Các virus khác | ||||
| 169 | Rotavirus test nhanh | |||
| Danh mục xét nghiệm KST | ||||
| A. Ký sinh trùng trong phân | ||||
| 178 | Hồng cầu, bạch cầu trong phân soi tươi | |||
| 179 | Hồng cầu trong phân test nhanh | |||
| 180 | Đơn bào đường ruột soi tươi | |||
| 181 | Đơn bào đường ruột nhuộm soi | |||
| 182 | Trứng giun, sán soi tươi | |||
| 183 | Trứng giun soi tập trung | |||
| 184 | Strongyloides stercoralis (giun lươn) ấu trùng soi tươi | |||
| B. Ký sinh trùng trong máu | ||||
| 192 | Plasmodium (Ký sinh trùng sốt rét) nhuộm soi định tính | |||
| C. Ký sinh trùng ngoài da | ||||
| 202 | Phthirus pubis (Rận mu) soi tươi | |||
| 203 | Phthirus pubis (Rận mu) nhuộm soi | |||
| 204 | Sarcoptes scabies hominis(Ghẻ) soi tươi | |||
| 205 | Sarcoptes scabies hominis(Ghẻ) nhuộm soi | |||
| Danh mục xét nghiệm Vi nấm | ||||
| 214 | Vi nấm soi tươi | |||
| 215 | Vi nấm test nhanh | |||
| 216 | Vi nấm nhuộm soi | |||
VI KHUẨN NHUỘM SOI
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đích
Nhận định sơ bộ hình ảnh vi khuẩn và các hình ảnh tế bào (nếu có) trực tiếp từ bệnh phẩm.
2. Nguyên lý
Đánh giá hình thể, kích thước, tính chất bắt màu, cách sắp xếp của vi khuẩn và các hình ảnh tế bào (nếu có) bằng kỹ thuật nhuộm và soi dưới kính hiển vi quang học.
II. CHUẨN BỊ
1. Người thực hiện
- Người thực hiện: Cán bộ xét nghiệm đã được đào tạo và có chứng chỉ hoc chứng nhận về chuyên ngành Vi
- Người nhận định và phê duyệt kết quả: cán bộ xét nghiệm có trình độ đại học hoặc sau đại học về chuyên ngành Vi
2. Phương tiện, hóa chất
Phương tiện, hóa chất như ví dụ dưới đây hoặc tương đương.
Trang thiết bị
- Máy ly tâm (cần cho một số loại bệnh phẩm)
- Tủ an toàn sinh học cấp 2
- Kính hiển vi quang học
- Dụng cụ sấy lam (nếu có)
Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
| STT | Chi phí hóa chất, vật tư tiêu hao | Đơn vị | Số lượng |
| 1 | Lọ lấy bệnh phẩm | Lọ | 1,000 |
| 2 | Que cấy | Cái | 1,000 |
| 3 | Lam kính | Cái | 2,000 |
| 4 | Dầu soi kính | ml | 1,000 |
| 5 | Cồn 96 độ lau kính | ml | 1,000 |
| 6 | Nước muối sinh lý | ml | 5,000 |
| 7 | Thuốc nhuộm đỏ fuchsin | ml | 5,000 |
| 8 | Thuốc nhuộm tím gentian | ml | 5,000 |
| 9 | Cồn tẩy 95% | ml | 10,000 |
| 10 | Lugol | ml | 5,000 |
| 11 | Thuốc nhuộm xanh methylen | ml | 5,000 |
| 12 | Bông | Kg | 0,001 |
| 13 | Cồn 90 độ (vệ sinh dụng cụ) | ml | 10,000 |
| 14 | Đèn cồn | Cái | 0,0001 |
| 15 | Panh | Cái | 0,0001 |
| 16 | Khay đựng bệnh phẩm | Cái | 0,0001 |
| 17 | Hộp vận chuyển bệnh phẩm | Cái | 0,0001 |
| 18 | Mũ | Cái | 0,020 |
| 19 | Khẩu trang | Cái | 0,020 |
| 20 | Găng tay | Đôi | 3,000 |
| 21 | Găng tay xử lý dụng cụ | Đôi | 0,020 |
| 22 | Quần áo bảo hộ | Bộ | 0,001 |
| 23 | Acid ngâm lam | ml | 10,000 |
| 24 | Ống nghiệm thủy tinh | Ống | 1,000 |
| 25 | Bút viết kính | Cái | 0,020 |
| 26 | Bút bi | Cái | 0,010 |
| 27 | Bật lửa | Cái | 0,010 |
| 28 | Sổ lưu kết quả xét nghiệm | Tờ | 0,001 |
| 29 | Cồn sát trùng tay nhanh | ml | 1,000 |
| 30 | Dung dịch nước rửa tay | ml | 8,000 |
| 31 | Khăn lau tay | Cái | 0,030 |
| 32 | Giấy trả kết quả xét nghiệm | Tờ | 2,000 |
| 33 | QC (nếu thực hiện) * | 0,1 | |
| 34 | EQAS (nếu thực hiện) * | 0,005 |
* Ghi chú:
- Chi phí nội kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình nội kiểm (QC) là 1/10 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lượng ≥ 10 mẫu cho 1 lần tiến hành kỹ thuật).
- Chi phí ngoại kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình ngoại kiểm (EQAS) là 1/200 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lần ngoại kiểm trung bình 2 lần/1 năm).
3. Bệnh phẩm
Các loại bệnh phẩm được chỉ định xét nghiệm vi khuẩn.
4. Phiếu xét nghiệm
Điền đầy đủ thông tin theo mẫu phiếu yêu cầu.
III. CÁC BƯỚC TIẾN HÀNH
Các bước tiến hành thực hiện theo phương tiện, hóa chất được ví dụ ở trên.
- Nhỏ dung dịch tím gentian, phủ kín nơi dàn đồ phiến, duy trì 1 – 2 phút
- Đổ dung dịch tím gentian, rửa tiêu bản dưới vòi nước chảy nhẹ
- Nhỏ dung dịch lugol, để 30 giây
- Đổ dung dịch lugol, rửa nước
- Tẩy màu: nhỏ vài giọt cồn 95% lên tiêu bản, nghiêng đi nghiêng lại để cho cồn chảy từ cạnh nọ sang cạnh kia. Khi thấy màu tím trên lam kính vừa phai hết thì rửa nước
- Nhỏ dung dịch đỏ fuchsin, để 1 – 2 phút
- Rửa nước kỹ, để khô tiêu bản, soi kính hiển
IV. NHẬN ĐỊNH KẾT QUẢ
Chỉ đọc kết quả khi QC đạt tiêu chuẩn.
1. Đánh giá hình ảnh vi khuẩn trên tiêu bản nhuộm Gram
- Soi dưới vật kính dầu (x100)
- Diễn giải và đọc kết quả:
Vi khuẩn Gram (+) bắt màu tím sẫm của gentian. Vi khuẩn Gram (-) bắt màu đỏ của fuchsin.
2. Đánh giá hình ảnh tế bào trên tiêu bản nhuộm đơn (nếu có).
V. NHỮNG SAI SÓT VÀ XỬ TRÍ
Gram dương giả: Tẩy cồn chưa đủ thời gian Gram âm giả:
+ Tuổi của mẫu cấy vi khuẩn ảnh hưởng lên tính chất nhuộm Gram ở các mẫu cấy vi khuẩn để thời gian quá lâu.
+ Tẩy cồn quá lâu và tráng không kỹ.
Nhuộm lại tiêu bản khi nghi ngờ kết quả không chính xác.
VI KHUẨN TEST NHANH
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đích
Xác định nhanh sự có mặt của vi khuẩn gây bệnh trong bệnh phẩm thông qua phát hiện sự có mặt của kháng nguyên vi khuẩn.
2. Nguyên lý
Phát hiện kháng nguyên vi khuẩn dựa trên phản ứng kết hợp đặc hiệu giữa kháng nguyên với kháng huyết thanh mẫu.
II. CHUẨN BỊ
1. Người thực hiện
- Người thực hiện: Cán bộ xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành Vi
- Người nhận định và phê duyệt kết quả: cán bộ xét nghiệm có trình độ đại học hoặc sau đại học về chuyên ngành Vi
2. Phương tiện, hóa chất
Phương tiện, hóa chất như ví dụ dưới đây hoặc tương đương.
Trang thiết bị
Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
| STT | Chi phí hóa chất, vật tư tiêu hao | Đơn vị | Số lượng |
| 1 | Bông | Kg | 0,001 |
| 2 | Dây garô | Cái | 0,001 |
| 3 | Cồn | ml | 1,000 |
| 4 | Bơm kim tiêm | Cái | 1,000 |
| 5 | Panh | Cái | 0,0001 |
| 6 | Khay đựng bệnh phẩm | Cái | 0,0001 |
| 7 | Hộp vận chuyển bệnh phẩm | Cái | 0,001 |
| 8 | Tube đựng bệnh phẩm | Cái | 1,000 |
| 9 | Sinh phẩm chẩn đoán | Test | 1,000 |
| 10 | Đầu côn 200 ul | Cái | 2,000 |
| 11 | Giấy thấm | Cuộn | 0,100 |
| 12 | Giấy xét nghiệm | Tờ | 2,000 |
| 13 | Sổ lưu kết quả xét nghiệm | Tờ | 0,001 |
| 14 | Bút viết kính | Cái | 0,020 |
| 15 | Bút bi | Cái | 0,010 |
| 16 | Mũ | Cái | 0,020 |
| 17 | Khẩu trang | Cái | 0,020 |
| 18 | Găng tay | Đôi | 0,100 |
| 19 | Găng tay xử lý dụng cụ | Đôi | 0,020 |
| 20 | Quần áo bảo hộ | Bộ | 0,005 |
| 21 | Dung dịch nước rửa tay | ml | 8,000 |
| 22 | Cồn sát trùng tay nhanh | ml | 1,000 |
| 23 | Dung dịch khử trùng | ml | 10,000 |
| 24 | Khăn lau tay | Cái | 0,010 |
| 25 | QC (nếu thực hiện) * | 0,1 | |
| 26 | EQAS (nếu thực hiện) * | 0,005 |
* Ghi chú:Thực hiện xét nghiệm 05 mẫu bệnh phẩm/lần.
- Chi phí nội kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình nội kiểm (QC) là 1/10 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lượng
≥ 10 mẫu cho 1 lần tiến hành kỹ thuật).
- Chi phí ngoại kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình ngoại kiểm (EQAS) là 1/200 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lần ngoại kiểm trung bình 2 lần/1 năm).
3. Bệnh phẩm
Các loại bệnh phẩm chỉ định làm test nhanh.
4. Phiếu xét nghiệm
Điền đầy đủ thông tin theo mẫu phiếu yêu cầu
III. CÁC BƯỚC THỰC HIỆN
Các bước tiến hành thực hiện theo phương tiện, hóa chất được ví dụ ở trên.
1. Lấy bệnh phẩm
Theo đúng quy định của chuyên ngành Vi sinh (Xem Phụ lục 1).
2. Tiến hành kỹ thuật
Bộ sinh phẩm Slidex Meningite – Kit 5 (VD) phát hiện 5 căn nguyên vi khuẩn gây viêm màng não.
| Các bước thực hiện | Kỹ thuật |
| 1. | Đưa sinh phẩm ra ngoài nhiệt độ phòng Đánh số thứ tự các bệnh phẩm và số thứ tự trên tấm kính |
| 2. | Lắc nhẹ nhàng lọ chứa hạt latex, không được lắc quá mạnh |
| 3. | Dùng pipet nhỏ 1 giọt dịch não tủy của người bệnh vào ô tương ứng đã đánh số trên phiến kính. Nhỏ chứng dương và chứng âm |
| 4. | Lắc nhẹ nhàng lọ có chứa hạt latex và nhỏ một giọt vào cạnh giọt dịch não tủy của người bệnh |
| 5. | Trộn đều 2 loại với nhau bằng que trộn phủ đều bề mặt của mỗi ô. |
| 6. | Lắc đều cả phiến kính bằng tay hoặc dùng máy lắc 80-100 vòng trong 10 phút |
| 7. | Đọc kết quả |
IV. NHẬN ĐỊNH KẾT QUẢ
- Ô chứng dương: có nhiện tượng ngưng kết hạt latex
- Ô chứng âm: không có nhiện tượng ngưng kết, hỗn dịch nhìn thấy mịn, đồng nhất
- Ô không có hiện tượng ngưng kết, hỗn dịch nhìn thấy mịn, đồng nhất: Âm tính
- Ô có hiện tượng ngưng kết, hỗn dịch nhìn thấy thô, có hạt ngưng kết rõ trên nền đen.
V. NHỮNG SAI SÓT VÀ XỬ TRÍ
Lượng bệnh phẩm đưa vào quá nhiều hoặc quá ít đều có thể ảnh hưởng đến kết quả.
Do vậy, phải tiến hành lấy thể tích bệnh phẩm đúng theo yêu cầu (Xem Phụ lục 6).
AFB TRỰC TIẾP NHUỘM ZIEHL-NEELSEN
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đích
Phát hiện các trực khuẩn bền vững với acid (AFB – acid fast bacillus) thuộc chi Mycobacterium.
2. Nguyên lý
Do đặc tính kháng acid của AFB nên khi được nhuộm bằng phương pháp Ziehl-Neelsen và soi dưới kính hiển vi quang học, hình ảnh của AFB sẽ có màu đỏ, các vi khuẩn và các tế bào (nếu có) không có đặc tính kháng acid sẽ có màu xanh.
II. CHUẨN BỊ
1. Người thực hiện
- Người thực hiện: Cán bộ xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành Vi
- Người nhận định và phê duyệt kết quả: cán bộ xét nghiệm có trình độ đại học hoặc sau đại học về chuyên ngành Vi
2. Phương tiện, hóa chất
Phương tiện, hóa chất như ví dụ dưới đây hoặc tương đương.
Trang thiết bị
- Tủ an toàn sinh học cấp 2
- Kính hiển vi quang học
- Thiết bị sấy lam (nếu có)
Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
| STT | Chi phí hóa chất, vật tư tiêu hao | Đơn vị | Số lượng |
| 1 | Dung dịch fuchsin 0,3% | ml | 5,000 |
| 2 | Dung dịch cồn tẩy HCL 3% | ml | 10,000 |
| 3 | Dung dịch xanh methylen 0,3% | ml | 5,000 |
| 4 | Cồn 96 độ (vệ sinh dụng cụ và ngâm lam) | ml | 20,000 |
| 5 | Dung dịch khử khuẩn ngâm que phết đờm | ml | 15,000 |
| 6 | Cồn sát trùng tay nhanh | ml | 2,000 |
| 7 | Dung dịch nước rửa tay | ml | 8,000 |
| 8 | Lọ/cốc/ tuýp lấy bệnh phẩm | Lọ | 1,200 |
| 9 | Que cấy | Cái | 1,000 |
| 10 | Lam kính | Cái | 1,500 |
| 11 | Que phết đờm | Cái | 1,500 |
| 12 | Dầu soi kính | ml | 1,000 |
| 13 | Giấy lau kính | Tờ | 2,000 |
| 14 | Bông | Kg | 0,001 |
| 15 | Đèn cồn | Cái | 0,0001 |
| 16 | Panh | Cái | 0,0001 |
| 17 | Khay đựng bệnh phẩm | Cái | 0,0001 |
| 18 | Hộp vận chuyển bệnh phẩm | Cái | 0,0001 |
| 19 | Hộp lưu tiêu bản | Cái | 0,0001 |
| 20 | Bô can (bình chứa) vật nhiễm | Cái | 0,0001 |
| 21 | Mũ | Cái | 0,020 |
| 22 | Khẩu trang | Cái | 0,020 |
| 23 | Găng tay | Đôi | 2,000 |
| 24 | Găng tay xử lý dụng cụ | Đôi | 0,020 |
| 25 | Quần áo bảo hộ | Bộ | 0,001 |
| 26 | Khăn lau tay | Cái | 0,030 |
| 27 | Túi chứa rác thải lây nhiễm | Cái | 0,0001 |
| 28 | Khăn giấy vệ sinh các bàn làm việc | Tờ | 2,000 |
| 29 | Bút viết kính | Cái | 0,020 |
| 30 | Bút bi | Cái | 0,010 |
| 31 | Bật lửa | Cái | 0,010 |
| 32 | Sổ nhận bệnh phẩm | Tờ | 0,001 |
| 33 | Sổ lưu kết quả xét nghiệm | Tờ | 0,001 |
| 34 | Sổ bàn giao kết quả xét nghiệm | Tờ | 0,001 |
| 35 | Giấy trả kết quả xét nghiệm | Tờ | 2,000 |
| 36 | Nhãn mã vạch | Cái | 3,000 |
| 37 | QC (nếu thực hiện) * | 0,1 | |
| 38 | EQAS (nếu thực hiện) * | 0,005 |
* Ghi chú:
- Chi phí nội kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình nội kiểm (QC) là 1/10 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lượng
≥ 10 mẫu cho 1 lần tiến hành kỹ thuật).
- Chi phí ngoại kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình ngoại kiểm (EQAS) là 1/200 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lần ngoại kiểm trung bình 2 lần/1 năm).
3. Bệnh phẩm
Đờm, dịch phế quản, phân, mủ, dịch não tủy, các loại dịch khác, …
4. Phiếu xét nghiệm
Điền đầy đủ thông tin theo mẫu yêu cầu
III. CÁC BƯỚC TIẾN HÀNH
Các bước tiến hành thực hiện theo phương tiện, hóa chất được ví dụ ở trên.
1. Lấy bệnh phẩm
Theo đúng quy định của chuyên ngành Vi sinh.
2. Tiến hành kỹ thuật
- Chuẩn bị tiêu bản đạt tiêu chuẩn của CTCLQG
- Cố định tiêu bản
- Nhỏ dung dịch fuchsin phủ kín nơi dàn đồ phiến, hơ nóng cho bốc hơi 3 lần (không được sôi)
- Rửa nước
- Tẩy màu bằng dung dịch cồn acid cho đến khi phai hết màu đỏ
- Rửa nước
- Nhỏ dung dịch xanh methylen phủ lên vùng dàn tiêu bản
- Đọc và đánh giá kết quả tiêu bản trên kính hiển vi quang học
IV. NHẬN ĐỊNH KẾT QUẢ
Quan sát AFB bằng vật kính dầu (x100) trên kính hiển vi quang học. AFB có hình ảnh trực khuẩn mảnh, hơi cong, bắt màu đỏ đứng riêng lẻ hay xếp đôi hoặc từng đám trên nền xanh. Đếm số lượng AFB và ghi kết quả như bảng sau:
| Số lượng AFB | Kết quả | Phân loại |
| Có > 10 AFB/ 1 vi trường (Soi ít nhất 20 vi trường) | Dương tính | 3 + |
| Có từ 1-10 AFB/ 1 vi trường (Soi ít nhất 50 vi trường) | Dương tính | 2 + |
| Có từ 10-99 AFB/ 100 vi trường | Dương tính | 1 + |
| Có từ 1-9 AFB/ 100 vi trường | Dương tính | Ghi số lượng cụ thể |
| Không AFB/ 100 vi trường | Âm tính | |
Lưu ý: 1 dòng tương đương 100 vi trường. Soi ít nhất 1 dòng (tiêu bản dương). Soi ít nhất 3 dòng (tiêu bản âm)
V. NHỮNG SAI SÓT VÀ XỬ TRÍ
- Mỗi mẻ nhuộm không nên quá 12 tiêu bản, các tiêu bản để cách nhau ít nhất 1
- Tiêu bản vẫn còn màu hồng do tẩy chưa đủ thời
- Tiêu bản có nhiều cặn fuchsin do chưa lọc hóa chất hoặc chai nhuộm không được súc rửa khi cho hóa chất mới.
- Tiêu bản nhìn không rõ vi trường có thể do để ngược tiêu bản, điều chỉnh kính hiển vi chưa đúng…
- AFB nhạt màu có thể do tẩy quá lâu hoặc nhuộm chưa đủ (thời gian, sức nóng).
- Nếu AFB tối màu có thể do nhuộm nền quá lâu.
- Tiêu bản có nhiều muội đen bám phía sau có thể do que đốt hết cồn.
AFB TRỰC TIẾP NHUỘM HUỲNH QUANG
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đích
Phát hiện các trực khuẩn bền vững với acid (AFB – acid fast bacillus) thuộc chi Mycobacterium.
2. Nguyên lý
Với kỹ thuật nhuộm huỳnh quang, AFB được phát hiện bởi hình thể trực khuẩn mảnh phát quang trên nền tối khi soi dưới kính hiển vi huỳnh quang.
II. CHUẨN BỊ
1. Người thực hiện
- Người thực hiện Cán bộ xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành Vi
- Người nhận định và phê duyệt kết quả: cán bộ xét nghiệm có trình độ đại học hoặc sau đại học về chuyên ngành Vi
2. Phương tiện, hóa chất
Phương tiện, hóa chất như ví dụ dưới đây hoặc tương đương.
Trang thiết bị
- Tủ an toàn sinh học cấp 2
- Kính hiển vi huỳnh quang đèn LED
- Thiết bị sấy lam (nếu có)
2.2. Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
| STT | Chi phí hóa chất, vật tư tiêu hao | Đơn vị | Số lượng |
| 1 | FAST Auramin O stain | ml | 1,300 |
| 2 | FAST Decolorizer | ml | 1,200 |
| 3 | Cồn 96 độ (vệ sinh dụng cụ và ngâm lam) | ml | 20,000 |
| 4 | Dung dịch khử khuẩn ngâm que phết đờm | ml | 15,000 |
| 5 | Cồn sát trùng tay nhanh | ml | 2,000 |
| 6 | Dung dịch nước rửa tay | ml | 8,000 |
| 7 | Lọ/cốc/ tuýp lấy bệnh phẩm | Lọ | 1,200 |
| 8 | Lam kính | Cái | 1,500 |
| 9 | Que phết đờm | Cái | 1,500 |
| 10 | Giấy lau kính | Tờ | 2,000 |
| 11 | Bông | Kg | 0,001 |
| 12 | Panh | Cái | 0,0001 |
| 13 | Khay đựng bệnh phẩm | Cái | 0,0001 |
| 14 | Hộp vận chuyển bệnh phẩm | Cái | 0,0001 |
| 15 | Hộp lưu tiêu bản | Cái | 0,0001 |
| 16 | Bô can (bình chứa) vật nhiễm | Cái | 0,0001 |
| 17 | Mũ | Cái | 0,020 |
| 18 | Khẩu trang | Cái | 0,020 |
| 19 | Găng tay | Đôi | 2,000 |
| 20 | Găng tay xử lý dụng cụ | Đôi | 0,020 |
| 21 | Quần áo bảo hộ | Bộ | 0,001 |
| 22 | Khăn lau tay | Cái | 0,030 |
| 23 | Túi chứa rác thải lây nhiễm | Cái | 0,0001 |
| 24 | Khăn giấy vệ sinh các bàn làm việc | Tờ | 2,000 |
| 25 | Bút viết kính | Cái | 0,020 |
| 26 | Bút bi | Cái | 0,010 |
| 27 | Sổ nhận bệnh phẩm | Tờ | 0,001 |
| 28 | Sổ lưu kết quả xét nghiệm | Tờ | 0,001 |
| 29 | Sổ bàn giao kết quả xét nghiệm | Tờ | 0,001 |
| 30 | Giấy trả kết quả xét nghiệm | Tờ | 2,000 |
| 31 | Nhãn mã vạch | Cái | 3,000 |
| 32 | QC (nếu thực hiện) * | 0,1 | |
| 33 | EQAS (nếu thực hiện) * | 0,005 |
Chi phí nội kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình nội kiểm (QC) là 1/10 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lượng* Ghi chú:
≥ 10 mẫu cho 1 lần tiến hành kỹ thuật).
- Chi phí ngoại kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình ngoại kiểm (EQAS) là 1/200 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lần ngoại kiểm trung bình 2 lần/1 năm).
3. Bệnh phẩm
Đờm, dịch phế quản, phân, mủ, dịch não tủy, các loại dịch khác, …
4. Phiếu xét nghiệm: Điền đầy đủ thông tin theo mẫu yêu cầu
III. CÁC BƯỚC TIẾN HÀNH
Các bước tiến hành thực hiện theo phương tiện, hóa chất được ví dụ ở trên.
1. Lấy bệnh phẩm
Theo đúng quy định của chuyên ngành Vi sinh (Xem Phụ lục 1).
2. Tiến hành kỹ thuật
- Chuẩn bị tiêu bản đạt tiêu chuẩn của CTCLQG
- Cố định tiêu bản
- Nhuộm màu bằng FAST Auramin O
- Tẩy và nhuộm nền bằng FAST Decolorizer
- Đọc và đánh giá kết quả trên kính hiển vi huỳnh quang đèn LED
IV. NHẬN ĐỊNH KẾT QUẢ
Quan sát AFB bằng vật kính 40 trên kính huỳnh quang đèn LED. AFB có hình ảnh trực khuẩn mảnh, hơi cong, đứng riêng lẻ, xếp đôi, song song hoặc từng đám. AFB bắt màu vàng sáng phát quang trên nền tối. Đếm số lượng AFB và ghi kết quả như bảng sau:
| Số lượng AFB | Kết quả | Mức độ |
| >50AFB/1 vi trường (Đọc ít nhất 8 vi trường) | Dương tính | 3 + |
| 5-50AFB/1 vi trường (Đọc ít nhất 20 vi trường) | Dương tính | 2+ |
| 20-199AFB/1 dòng (Đọc ít nhất 1 dòng) | Dương tính | 1 + |
| 1-19AFB /1 dòng | Dương tính | Ghi số lượng cụ thể |
| 0 AFB /ít nhất 1 dòng | Âm tính | |
Lưu ý: 1 dòng lam tương đương 40 vi trường.
V. NHỮNG SAI SÓT VÀ XỬ TRÍ
- Mỗi mẻ nhuộm không nên quá 12 tiêu bản, các tiêu bản để cách nhau ít nhất 1
- AFB phát quang yếu có thể do tiêu bản sau khi nhuộm không đọc ngay, tiêu bản bị tiếp xúc nhiều với ánh sáng.
- AFB phát quang yếu có thể do chất lượng hóa chất không đạt do bảo quản chưa đúng, quá hạn
MYCOBACTERIUM TUBERCULOSIS NUÔI CẤY MÔI TRƯỜNG LỎNG
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đích
Phát hiện Mycobacterium tuberculosis bằng kỹ thuật nuôi cấy môi trường lỏng.
2. Nguyên lý
Tube MGIT chứa môi trường lỏng Middlebrook 7H9 có oxy hòa tan và 1 hợp chất gồm: chất màu huỳnh quang, tris 4, 7-diphenyl-1, 10-phenonthroline ruthenium chloride pentahydrate được gắn vào lớp silicone ở đáy tube. Khi vi khuẩn phát triển oxy bị tiêu thụ, nồng độ oxy giảm, chất màu huỳnh quang thoát ức chế sẽ phát quang trong tube MGIT, có thể quan sát bằng tia UV. Cường độ phát quang tương ứng với mức độ tiêu thụ oxy, tương ứng nồng độ vi khuẩn phát triển trong tube môi trường. Máy tự động giám sát sự phát quang 60 phút một lần. Vi khuẩn mọc càng nhiều càng tăng độ phát quang.
II. CHUẨN BỊ
1. Người thực hiện
- Người thực hiện: Cán bộ xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành Vi
- Người nhận định và phê duyệt kết quả: Cán bộ xét nghiệm có trình độ đại học hoặc sau đại học về chuyên ngành Vi
2. Phương tiện, hóa chất
Phương tiện, hóa chất như ví dụ dưới đây hoặc tương đương.
Trang thiết bị
- Tủ an toàn sinh học cấp 2
- Máy li tâm đủ tiêu chuẩn an toàn sinh học, đủ lực ly tâm (>= 3000 g).
- Máy lắc: vortex
- Tủ lạnh
- Cân điện tử: max 220 g, d = 0,1 mg
- Đồng hồ phút
- Kính hiển vi
- Nồi hấp
- Hệ thống máy BACTEC- MGIT 960 hoặc 320
- Pipet loại 100-1000
Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
| STT | Chi phí hóa chất, vật tư tiêu hao | Đơn vị | Số lượng |
| I | Hoá chất | ||
| 1 | MGIT tuýp loại 7 ml | tuýp | 1,100 |
| 2 | MGIT supplement – PANTA | ml | 0,900 |
| 3 | KH2PO4 | gam | 0,250 |
| 4 | Na2HPO4 | gam | 0,250 |
| 5 | Cồn 700 | ml | 5,000 |
| 6 | Nước cất | ml | 60,000 |
| 7 | NaOH | gam | 0,020 |
| 8 | NaCitrat | gam | 0,015 |
| 9 | NALC | mg | 25,000 |
| 10 | Dầu soi | ml | 0,100 |
| 11 | Cồn 950 | ml | 4,500 |
| 12 | Cacbol fuchsin | gam | 0,030 |
| 13 | HCL | ml | 0,300 |
| 14 | Phenol | ml | 0,500 |
| 15 | Methylen | gam | 0,030 |
| 16 | Thanh định danh nhanh ( SD, TBcID..) | test | 0,400 |
| 17 | Presept 2,5 | viên | 0,050 |
| 18 | Microshiel | ml | 1,000 |
| 19 | Lòng trắng trứng | ml | 0,010 |
| II | Vật tư tiêu hao | ||
| 20 | Lam kính | cái | 2,200 |
| 21 | Tuyp nắp xoáy vô trùng 50ml | cái | 1,100 |
| 22 | Pipette Paster nhựa vô trùng | cái | 3,000 |
| 23 | Chai thủy tinh trung tính 1000ml | cái | 0,001 |
| 24 | Que phết đờm | cái | 0,500 |
| 25 | Giấy lau kính hiển vi | tờ | 0,100 |
| 26 | Bông thấm nước | gam | 0,500 |
| 27 | Đầu côn nhựa loại 1ml | cái | 0,010 |
| 28 | Găng tay | đôi | 0,200 |
| 29 | Tuýp 18 x 24 mm | cái | 0,100 |
| 30 | Bô can | cái | 0,010 |
| 31 | Hộp đựng tiêu bản | cái | 0,001 |
| 32 | Túi nilon loại 2 loại chịu nhiệt hấp | cái | 0,050 |
| 33 | Túi rác vàng hủy vật liệu lây nhiễm | cái | 0,020 |
| 34 | Thùng rác có nắp | cái | 0,001 |
| 35 | Thùng vận chuyển vật liệu lây nhiễm | cái | 0,001 |
| 36 | Hộp đựng vật sắc nhọn | cái | 0,003 |
| 37 | Khay đựng bệnh phẩm | cái | 0,001 |
| 38 | Hộp vận chuyển bệnh phẩm | cái | 0,001 |
| 39 | Giá đựng tuýp | cái | 0,001 |
| 40 | Mũ | cái | 0,020 |
| 41 | Khẩu trang | cái | 0,020 |
| 42 | Găng tay xử lý dụng cụ | Đôi | 0,020 |
| 43 | Quần áo bảo hộ | Bộ | 0,001 |
| 44 | Dung dịch tẩy rửa dụng cụ | ml | 10,000 |
| 45 | Bút chì đen HB | cái | 0,020 |
| 46 | Bút bi | cái | 0,010 |
| 47 | Bật lửa | cái | 0,010 |
| 48 | Sổ lưu kết quả xét nghiệm | Tờ | 0,001 |
| 49 | Khăn lau tay | cái | 0,005 |
| 50 | Giấy trả kết quả xét nghiệm | Tờ | 2,000 |
| 51 | Nhãn mã vạch | cái | 4,000 |
| 52 | QC (nếu thực hiện) * | 0,1 | |
| 53 | EQAS (nếu thực hiện) * | 0,005 |
* Ghi chú:
- Chi phí nội kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình nội kiểm (QC) là 1/10 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lượng ≥ 10 mẫu cho 1 lần tiến hành kỹ thuật).
- Chi phí ngoại kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình ngoại kiểm (EQAS) là 1/200 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lần ngoại kiểm trung bình 2 lần/1 năm).
3. Bệnh phẩm
Đờm, dịch phế quản, phân, mủ, dịch não tủy, các loại dịch khác…
4. Phiếu xét nghiệm
Điền đầy đủ thông tin theo mẫu yêu cầu
III. CÁC BƯỚC TIẾN HÀNH
Các bước tiến hành thực hiện theo phương tiện, hóa chất được ví dụ ở trên.
1. Lấy bệnh phẩm
Theo đúng quy định của chuyên ngành Vi sinh (Xem Phụ lục 1 và Phụ lục 4).
2. Tiến hành kỹ thuật
Chuẩn bị môi trường hóa chất
Xử lý bệnh phẩm, nhuộm soi, nuôi cấy
Định danh: soi định danh và định danh nhanh bằng sắc kí miễn dịch
Xử lý vật liệu lây nhiễm
IV. NHẬN ĐỊNH KẾT QUẢ
- Kết quả nhuộm soi tìm AFB (hướng dẫn của Chương trình chống lao Quốc gia)
| Số lượng AFB | Kết quả | Phân loại |
| Có > 10 AFB/ 1 vi trường (Soi ít nhất 20 vi trường) | Dương tính | AFB 3 (+) |
| Có từ 1-10 AFB/ 1 vi trường (Soi ít nhất 50 vi trường) | Dương tính | AFB 2 (+) |
| Có từ 10-99 AFB/ 100 vi trường | Dương tính | AFB 1 (+) |
| Có từ 1-9 AFB/ 100 vi trường | Dương tính | Ghi số lượng AFB/100 vi trường |
| Không AFB/ 100 vi trường | Âm tính | |
2. Kết quả cấy
- Kết quả cấy dương tính trung bình trong vòng 3 ngày đến 2 tuần: máy tự động đọc và báo kết quả dương tính bằng tín hiệu đèn đỏ và âm thanh, lấy tuýp cấy được máy báo dương ra khỏi máy để định
- Kết quả cấy âm tính được máy báo bằng tín hiệu đèn xanh và âm thanh sau 6 tuần, lấy tuýp cấy được máy báo âm ra khỏi máy quan sát bằng mắt thường để phát hiện tube cấy dương (có cặn vụn) trước khi khẳng định cấy âm tránh bỏ sót các trường hợp cấy dương tính máy không phát hiện được do số lượng vi khuẩn mọc ít.
- Ngoài ra tube cấy máy báo âm tính có đầu vào nhuộm soi dương phải ly tâm lấy cặn nhuộm soi để kiểm tra kết quả.
3. Kết quả định danh
Soi định danh
Các tube cấy do máy báo dương hoặc quan sát bằng mắt thấy cặn vụn hút cặn làm tiêu bản nhuộm ZN soi định danh gặp các tình huống sau:
- AFB dạng cuộn thừng nghĩ đến tuberculosis (MTB)
- AFB hình thể vụn xếp thành đám nghĩ đến NTM
- AFB tạo dạng cuộn thừng lẫn AFB hình thể vụn: nghĩ đến mẫu cấy vừa có MTB vừa có NTM
- AFB dạng cuộn thừng lẫn vi khuẩn khác: mẫu cấy có MTB và ngoại nhiễm
- Không có AFB, có các vi khuẩn khác hoặc nấm mẫu cấy bị ngoại nhiễm
- Soi không thấy gì tiếp tục ủ ấm làm tiêu bản khác sau 3 ngày.
Định danh nhanh bằng sắc ký miễn dịch (SD, TBcID..)
Những tuýp cấy dương tiến hành soi AFB, định danh nhanh bằng sắc ký miễn dịch (SD, TBcID..) để khẳng định M. tuberculosis complex.
- tuberculosis complex có kết quả định danh MTB dương tính
- NTM có kết quả định danh MTB âm tính
V. NHỮNG SAI SÓT VÀ XỬ TRÍ
Máu lẫn trong bệnh phẩm ảnh hưởng đến kết quả cấy, vì vậy các bệnh phẩm lẫn nhiều máu không nuôi cấy lỏng yêu cầu lấy bệnh phẩm khác. Trường hợp dịch lẫn ít máu (tuýp dịch phân thành 2 lớp: dịch trên máu dưới) gạn lấy phần dịch thêm nước cất để phá vỡ hồng cầu trước khi Xử lý.
Nhiễm chéo trong quá trình thao tác kỹ thuật: hạn chế nhiễm chéo bằng cách phân loại nguồn bệnh phẩm dịch, đờm, nghi MDR, người bệnh thường…để Xử lý thích hợp. Không cấy chuyển chủng không làm tiêu bản soi định danh cùng lúc Xử lý bệnh phẩm. Chia nhỏ hóa chất dung dịch đệm, thao tác nhẹ nhàng tránh tạo hạt mù, chắt dung dịch vào thành tuýp. Không mở đồng thời các tuýp mẫu Mỗi mẻ Xử lý 6 – 8 mẫu.
Tỷ lệ ngoại nhiễm cao: giảm ngoại nhiễm bằng cách: Xử lý mẫu càng sớm càng tốt. Mẫu bảo quản 2 – 8 0 C không quá 72 giờ, dịch dạ dày, nước tiểu Xử lý sớm trước 4 giờ kể từ khi lấy mẫu. Tuân thủ quy trình xử lý, nồng độ và thời gian tiếp xúc với hóa chất. Đảm bảo chất lượng môi trường, sinh phẩm, hóa chất, dụng cụ trong hạn và vô trùng.
Nhầm lẫn hành chính: Kiểm tra cẩn thận về hành chính từ khâu nhận bệnh phẩm, vào sổ, trả kết quả, tránh nhầm lẫn. Khi thao tác kỹ thuật xếp mẫu theo thứ tự, tuân thủ qui tắc để cách ô trống đầu tiên.
Mycobacterium tuberculosis Mantoux
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đích
Phát hiện nhiễm Mycobacterium tuberculosis.
2. Nguyên lý
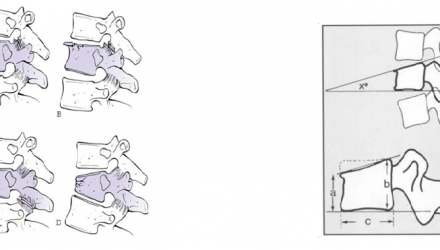
Phản ứng Mantoux bản chất là phản ứng quá mẫn muộn với tuberculin. Tiêm trong da 0.1 ml Tuberculin PPD (protein tinh khiết chiết tách từ vi khuẩn lao) cho người được chỉ định, nếu bị nhiễm lao sẽ có phản ứng dị ứng quá mẫn muộn (sau khi tiêm 72 giờ) tại nơi tiêm. Đọc kết quả phản ứng bằng cách xác định và đo đường kính cục sần hoặc vết phồng rộp.
II. CHUẨN BỊ
1. Người thực hiện
- Người thực hiện: Cán bộ xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành Vi
- Người nhận định và phê duyệt kết quả: Cán bộ xét nghiệm có trình độ đại học hoặc sau đại học về chuyên ngành Vi
2. Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
Phương tiện, hóa chất như ví dụ dưới đây hoặc tương đương.
| STT | Chi phí hóa chất, vật tư tiêu hao | Đơn vị | Số lượng |
| I | Hoá chất | ||
| 1 | Tuberculin Tuỳ hãng sản xuất, có loại dung dịch, có loại đông khô và dung môi. | ml | 0,150 |
| 2 | Cồn 70 | ml | 0,300 |
| 3 | Microshiel | ml | 1,000 |
| II | Vật tƣ tiêu hao | ||
| 4 | Bơm tiêm loại 1ml | cái | 1,100 |
| 5 | Kim tiêm cỡ 25 – 26 | cái | 1,100 |
| 6 | Bông thấm nước | gr | 0,050 |
| 7 | Hộp inox đựng bông cồn | cái | 0,001 |
| 8 | Khay inox | cái | 0,001 |
| 9 | Kéo | cái | 0,001 |
| 10 | Panh | cái | 0,001 |
| 11 | Túi rác vàng hủy vật liệu lây nhiễm | cái | 0,020 |
| 12 | Thùng rác có nắp | cái | 0,001 |
| 13 | Hộp đựng vật sắc nhọn | cái | 0,003 |
| 14 | Thước nhựa trong, mềm có chia vạch mm | cái | 0,001 |
| 15 | Mũ | cái | 0,020 |
| 16 | Khẩu trang | cái | 0,020 |
| 17 | Găng tay | Đôi | 0,020 |
| 18 | Quần áo bảo hộ | Bộ | 0,001 |
| 19 | Bút bi | cái | 0,010 |
| 20 | Sổ lưu kết quả xét nghiệm | Tờ | 0,001 |
| 21 | Khăn lau tay | cái | 0,005 |
| 22 | Giấy trả kết quả xét nghiệm | Tờ | 2,000 |
3. Bệnh phẩm
Người được chỉ định xét nghiệm
4. Phiếu xét nghiệm
Điền đầy đủ thông tin theo mẫu yêu cầu
III. CÁC BƯỚC TIẾN HÀNH
Các bước tiến hành thực hiện theo phương tiện, hóa chất được ví dụ ở trên.
1. Chuẩn bị sinh phẩm
2. Tiến hành kỹ thuật
3. Dặn dò, hẹn người bệnh đến đọc kết quả
4. Đọc kết quả
5. Xử lý vật liệu lây nhiễm
IV. NHẬN ĐỊNH KẾT QUẢ
1. Đọc kết quả
Quan sát cục sần, hiện tượng phồng, rộp, đo đường kính cục sần, tính ra mm.
3. Diễn giải kết quả
Biện luận kết quả phụ thuộc vào loại tuberculin và hướng dẫn của nhà sản xuất. Ví dụ Tuberculin RT23 SSI chuẩn quốc tế do viện Statens Serum của Đan Mạch sản xuất: Liều tiêm 02 đơn vị (2TU/ 0,1ml = 0,04 microgam tuberculin PPD)
| Đường kính cục sần | ||
| Âm tính: 0-5mm | Dương tính: 6-14mm | Dương tính mạnh: ≥ 15 mm |
Kết quả dương tính thể hiện đáp ứng miễn dịch theo một trong các tình huống sau:
- Nhiễm Mycobacterium tuberculosis
- Nhiễm
- Tiền sử tiêm BCG (thường sau 4-8 tuần).
Phản ứng dương tính mạnh thường do nhiễm Mycobacterium tuberculosis complex.
V. NHỮNG SAI SÓT VÀ XỬ TRÍ
- Phản ứng âm tính giả: Là phản ứng âm tính trong khi người thử phản ứng có mắc bệnh lao: Thể lao tiến triển nặng (lao kê, lao màng não…) phản ứng bị ức chế hoặc
- Tiêm không đúng kỹ thuật, tuberculin bảo quản không đúng qui định về nhiệt độ và thời
- Trong vòng một tháng sau khi người bệnh tiêm vắc xin có chứa virus sống (sởi, quai bị, rubella)
- Người bệnh bị các bệnh nhiễm virus (rubella, cúm,…)
- Người bệnh bị bệnh có suy giảm miễn dịch: Hodgkin, sarcoidosis, HIV
- Người bệnh rối loạn chuyển hoá nặng: Suy thận mãn, suy kiệt thiếu protein, bỏng nặng…
- Người bệnh già hoặc bệnh nhi dưới 6 tuần tuổi.
- Phản ứng dương tính giả: Là phản ứng dương tính trong khi người được thử phản ứng không bị nhiễm lao ( tuberculosis): Phản ứng chéo với các NTM.
3. Hiệu ứng không mong muốn
- Dị ứng có thể xảy ra với cá nhân mẫn cảm với thành phần thuốc thử. Chống chỉ định với người bệnh có tiền sử dị ứng với các thành phần thuốc thử tuberculin. Mặc dù rất hiếm, song cần phải có thuốc cấp cứu trong khi thử Mantoux
- Những cá nhân quá nhạy cảm loét, hoại tử tạo thành sẹo tại chỗ tiêm
- Có thể gặp đau đầu, sốt, nổi hạch nách.
- Có thể xảy ra sưng tấy, đau, ngứa, khó chịu ngay sau khi tiêm
Mycobacterium leprae nhuộm soi
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đích
Phát hiện các trực khuẩn Mycobacterium leprae còn goi là Bacillus Hansen (BH) bền vững với acid.
2. Nguyên lý
Do đặc tính kháng acid của Mycobacterium leprae nên khi được nhuộm bằng thuật nhuộm Ziehl-Neelsen và soi dưới kính hiển vi quang học, hình ảnh của Mycobacterium leprae sẽ có màu đỏ, các vi khuẩn và các tế bào (nếu có) không có đặc tính kháng acid sẽ xanh.
II. CHUẨN BỊ
1. Người thực hiện
- Người thực hiện Cán bộ xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành Vi
- Người nhận định và phê duyệt kết quả: Cán bộ xét nghiệm có trình độ đại học hoặc sau đại học về chuyên ngành Vi
2. Phương tiện, hóa chất
Phương tiện, hóa chất như ví dụ dưới đây hoặc tương đương.
Trang thiết bị
- Tủ an toàn sinh học cấp 2
- Kính hiển vi quang học
- Dụng cụ sấy lam (nếu có)
- Cán dao rạch da số 3 (Inox)
Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
| STT | Chi phí hóa chất, vật tư tiêu hao | Đơn vị | Số lượng |
| 1 | Lưỡi dao rạch da số 15 | Cái | 2,000 |
| 2 | Lam kính | Cái | 2,000 |
| 3 | Dầu soi kính | ml | 1,000 |
| 4 | Xylen lau kính | ml | 1,000 |
| 5 | Dung dịch fuchsin 1% | ml | 5,000 |
| 6 | Dung dịch cồn tẩy HCL 1% | ml | 10,000 |
| 7 | Dung dịch xanh methylen 0,2% | ml | 5,000 |
| 8 | Bông | Kg | 0,001 |
| 9 | Cồn 90 độ (vệ sinh dụng cụ) | ml | 10,000 |
| 10 | Đèn cồn | Cái | 0,0001 |
| 11 | Panh | Cái | 0,0001 |
| 12 | Khay đựng bệnh phẩm | Cái | 0,0001 |
| 13 | Hộp vận chuyển bệnh phẩm | Cái | 0,0001 |
| 14 | Mũ | Cái | 0,020 |
| 15 | Khẩu trang | Cái | 0,200 |
| 16 | Găng tay xử lý dụng cụ | Đôi | 0,0200 |
| 17 | Quần áo bảo hộ | Bộ | 0,0010 |
| 18 | Hộp đựng dung dịch khử khuẩn ngâm lưỡi dao | ||
| 19 | Bút viết kính | Cái | 0,020 |
| 20 | Bút bi | Cái | 0,010 |
| 21 | Bật lửa | Cái | 0,010 |
| 22 | Sổ lưu kết quả xét nghiệm | Tờ | 0,01 |
| 23 | Cồn sát trùng tay nhanh | ml | 2,000 |
| 24 | Dung dịch nước rửa tay | ml | 8,000 |
| 25 | Khăn lau tay | Cái | 0,300 |
| 26 | Giấy trả kết quả xét nghiệm | Tờ | 2,000 |
| 27 | QC (nếu thực hiện) * | 0,1 | |
| 28 | EQAS (nếu thực hiện) * | 0,005 |
* Ghi chú:
- Chi phí nội kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình nội kiểm (QC) là 1/10 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lượng ≥ 10 mẫu cho 1 lần tiến hành kỹ thuật).
- Chi phí ngoại kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình ngoại kiểm (EQAS) là 1/200 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lần ngoại kiểm trung bình 2 lần/1 năm).
3. Bệnh phẩm
Chất tiết và tế bào dưới da ở vị trí: dái tai, tổn thương
4. Phiếu xét nghiệm
Điền đầy đủ thông tin theo mẫu yêu cầu
III. CÁC BƯỚC TIẾN HÀNH
Các bước tiến hành thực hiện theo phương tiện, hóa chất được ví dụ ở trên.
1. Lấy bệnh phẩm
Theo đúng quy định của chuyên ngành Vi sinh (Xem Phụ lục 1 và Phụ lục 6)
2. Tiến hành kỹ thuật
Chuẩn bị tiêu bản
Nhuộm Fuchsin
Tẩy màu bằng dung dịch cồn acid
Nhuộm nền bằng dung dịch xanh methylen
IV. NHẬN ĐỊNH KẾT QUẢ
BH có hình ảnh trực khuẩn mảnh, hơi cong, bắt màu đỏ đứng riêng lẻ hay xếp đôi hoặc từng đám trên nền xanh. Đếm số lượng BH và ghi kết quả như bảng sau:
| Số lượng BH | Kết quả | Phân loại |
| Có từ 1-10 BH/ 100 vi trường | Dương tính | BH 1 (+) |
| Có từ 1-10 BH/ 10 vi trường | Dương tính | BH 2 (+) |
| Có từ 1-10 BH/ 1 vi trường | Dương tính | BH 3 (+) |
| Có từ 1-100 BH/ 1 vi trường | Dương tính | BH 4 (+) |
| Có từ 100 -1000 BH/ 1 vi trường | Dương tính | BH 5 (+) |
| Có >1000 BH/ 1 vi trường | Dương tính | BH 6 (+) |
| Không thấy BH/ 100 vi trường | Âm tính |
Lưu ý: 1 dòng lam tương đương 100 vi trường. Soi ít nhất 3 dòng.
V. NHỮNG SAI SÓT VÀ X TRÍ
1. Bệnh phẩm
Phòng xét nghiệm sẽ yêu cầu lấy lại bệnh phẩm khi phát hiện bệnh phẩm lấy, vận chuyển, bảo quản không đúng qui định. Nếu lâm sàng vẫn yêu cầu, phòng xét nghiệm sẽ thông báo mức độ kém chính xác của kết quả xét nghiệm.
2. Kỹ thuật
- BH nhạt màu có thể do tẩy quá lâu hoặc nhuộm chưa đủ (thời gian, sức nóng).
- Nếu BH tối màu có thể do nhuộm nền quá lâu.
- Mỗi mẻ nhuộm không nên quá 12 tiêu bản, các tiêu bản để cách nhau ít nhất 1
Vibrio cholerae nhuộm soi
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đích
Nhận định sơ bộ hình ảnh vi khuẩn vi khuẩn thuộc chi Vibrio trực tiếp từ bệnh phẩm.
2. Nguyên lý
Đánh giá hình thể, kích thước, tính chất bắt màu bằng kỹ thuật nhuộm và soi dưới kính hiển vi quang học.
II. CHUẨN BỊ
Phương tiện, hóa chất như ví dụ dưới đây hoặc tương đương.
1. Người thực hiện
- Người thực hiện Cán bộ xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành Vi
- Người nhận định và phê duyệt kết quả: Cán bộ xét nghiệm có trình độ đại học hoặc sau đại học về chuyên ngành Vi
2. Phương tiện, hóa chất
Trang thiết bị
- Tủ an toàn sinh học cấp 2
- Kính hiển vi quang học
- Dụng cụ sấy lam (nếu có)
Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
| STT | Chi phí hóa chất, vật tư tiêu hao | Đơn vị | Số lượng |
| 1 | Lọ lấy bệnh phẩm | lọ | 1,000 |
| 2 | Que lấy bệnh phẩm | cái | 1,000 |
| 3 | Lam kính | cái | 2,000 |
| 4 | Dầu soi kính | ml | 1,000 |
| 5 | Xylen lau kính | ml | 1,000 |
| 6 | Nước muối sinh lý | ml | 5,000 |
| 7 | Thuốc nhuộm đỏ fuchsin | ml | 5,000 |
| 8 | Thuốc nhuộm tím gentian | ml | 5,000 |
| 9 | Cồn tẩy 95 độ | ml | 10,000 |
| 10 | Lugol | ml | 5,000 |
| 11 | Bông | kg | 0,001 |
| 12 | Cồn 90 độ (vệ sinh dụng cụ) | ml | 10,000 |
| 13 | Đèn cồn | cái | 0,0001 |
| 14 | Panh | cái | 0,0001 |
| 15 | Khay đựng bệnh phẩm | cái | 0,0001 |
| 16 | Hộp vận chuyển bệnh phẩm | cái | 0,0001 |
| 17 | Mũ | cái | 0,020 |
| 18 | Khẩu trang | cái | 0,020 |
| 19 | Găng tay | đôi | 3,000 |
| 20 | Găng tay xử lý dụng cụ | đôi | 0,020 |
| 21 | Quần áo bảo hộ | bộ | 0,001 |
| 22 | Acid ngâm lam | ml | 10,000 |
| 23 | Ống nghiệm thủy tinh | ống | 1,000 |
| 24 | Bút viết kính | cái | 0,020 |
| 25 | Bút bi | cái | 0,010 |
| 26 | Bật lửa | cái | 0,010 |
| 27 | Sổ lưu kết quả xét nghiệm | tờ | 0,001 |
| 28 | Cồn sát trùng tay nhanh | ml | 2,000 |
| 29 | Dung dịch nước rửa tay | ml | 8,000 |
| 30 | Khăn lau tay | cái | 0,030 |
| 31 | Giấy trả kết quả xét nghiệm | tờ | 2,000 |
| 32 | QC (nếu thực hiện) * | 0,1 | |
| 33 | EQAS (nếu thực hiện) * | 0,005 |
* Ghi chú:
- Chi phí nội kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình nội kiểm (QC) là 1/10 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lượng ≥ 10 mẫu cho 1 lần tiến hành kỹ thuật).
- Chi phí ngoại kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình ngoại kiểm (EQAS) là 1/200 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lần ngoại kiểm trung bình 2 lần/1 năm).
3. Bệnh phẩm
Phân của người bệnh.
4. Phiếu xét nghiệm
Điền đầy đủ thông tin theo mẫu yêu cầu
III. CÁC BƯỚC TIẾN HÀNH
Các bước tiến hành thực hiện theo phương tiện, hóa chất được ví dụ ở trên.
1. Lấy bệnh phẩm
Theo đúng quy định của chuyên ngành Vi sinh (Xem Phụ lục 1).
2. Tiến hành kỹ thuật
Chuẩn bị tiêu bản
Nhuộm
- Nhuộm tím gentian trong vòng 60 giây
- Đổ toàn bộ phần thuốc nhuộm thừa rồi rửa nhẹ tiêu bản dưới vòi nước chảy
- Hỗ trợ bắt màu tím bằng lugol trong vòng 30 giây
- Đổ toàn bộ phần lugol thừa rồi rửa nhẹ tiêu bản dưới vòi nước chảy
- Tẩy màu bằng cồn 95% cho đến khi vừa hết màu tím phai ra
- Đổ toàn bộ phần cồn thừa rồi rửa nhẹ tiêu bản dưới vòi nước chảy
- Nhuộm tương phản bằng fuchsin trong vòng 60 giây
- Đổ toàn bộ phần thuốc nhuộm thừa rồi rửa nhẹ tiêu bản dưới vòi nước chảy
- Để tiêu bản khô và
IV. NHẬN ĐỊNH KẾT QUẢ
Vibrio cholerae có hình ảnh phẩy khuẩn, bắt màu Gram âm (màu đỏ). Khi có hình ảnh nghi ngờ trên tiêu bản nhuộm soi, cần đề nghị nuôi cấy để chẩn đoán xác định.
V. NHỮNG SAI SÓT VÀ XỬ TRÍ
1. Sai sót
- Vibrio cholerae có thể bắt màu không đúng do tẩy cồn chưa đủ hoặc làm lam quá dầy; thuốc nhuộm không đảm bảo chất lượng.
- Một số trường hợp trực khuẩn do cố định quá lâu tạo hình ảnh gần giống phẩy khuẩn.
2. Xử trí
- Tuân thủ đúng các bước của quy trình nhuộm
- Kiểm tra chất lượng thuốc nhuộm hàng tuần với chủng chuẩn.
Vibrio cholerae nhuộm huỳnh quang
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đích
Phát hiện nhanh Vibrio cholerae từ bệnh phẩm.
2. Nguyên lý
Nếu trong bệnh phẩm có V. cholerae, vi khuẩn sẽ kết hợp với kháng thể đặc hiệu gắn huỳnh quang. Khi soi dưới kính hiển vi huỳnh quang sẽ thấy hình ảnh phẩy khuẩn phát sáng màu vàng xanh.
II. CHUẨN BỊ
1. Người thực hiện
- Người thực hiện Cán bộ xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành Vi
- Người nhận định và phê duyệt kết quả: Cán bộ xét nghiệm có trình độ đại học hoặc sau đại học về chuyên ngành Vi
2. Phương tiện, hóa chất
Phương tiện, hóa chất như ví dụ dưới đây hoặc tương đương.
Trang thiết bị
- Tủ an toàn sinh học cấp 2
- Kính hiển vi huỳnh quang
- Dụng cụ sấy lam (nếu có)
Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
| STT | Chi phí hóa chất, vật tư tiêu hao | Đơn vị | Số lượng |
| 1 | Lọ lấy bệnh phẩm | lọ | 1,000 |
| 2 | Que lấy bệnh phẩm | cái | 1,000 |
| 3 | Lam kính | cái | 1,000 |
| 4 | Nước muối sinh lý | ml | 3,000 |
| 5 | Thuốc nhuộm Cholerae DFA | ml | 3,000 |
| 6 | Bông | kg | 0,001 |
| 7 | Cồn 90 độ (vệ sinh dụng cụ) | ml | 10,000 |
| 8 | Đèn cồn | cái | 0,0001 |
| 9 | Panh | cái | 0,0001 |
| 10 | Khay đựng bệnh phẩm | cái | 0,0001 |
| 11 | Hộp vận chuyển bệnh phẩm | cái | 0,0001 |
| 12 | Mũ | cái | 0,020 |
| 13 | Khẩu trang | cái | 0,020 |
| 14 | Găng tay | đôi | 3,000 |
| 15 | Găng tay xử lý dụng cụ | đôi | 0,020 |
| 16 | Quần áo bảo hộ | bộ | 0,001 |
| 17 | Acid ngâm lam | ml | 10,000 |
| 18 | Ống nghiệm thủy tinh | ống | 1,000 |
| 19 | Bút viết kính | cái | 0,020 |
| 20 | Bút bi | cái | 0,010 |
| 21 | Bật lửa | cái | 0,010 |
| 22 | Sổ lưu kết quả xét nghiệm | tờ | 0,001 |
| 23 | Cồn sát trùng tay nhanh | ml | 2,000 |
| 24 | Dung dịch nước rửa tay | ml | 8,000 |
| 25 | Khăn lau tay | cái | 0,030 |
| 26 | Giấy trả kết quả xét nghiệm | tờ | 2,000 |
| 27 | QC (nếu thực hiện) * | 0,1 | |
| 28 | EQAS (nếu thực hiện) * | 0,005 |
* Ghi chú:
- Chi phí nội kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình nội kiểm (QC) là 1/10 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lượng ≥ 10 mẫu cho 1 lần tiến hành kỹ thuật).
- Chi phí ngoại kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình ngoại kiểm (EQAS) là 1/200 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lần ngoại kiểm trung bình 2 lần/1 năm).
3. Bệnh phẩm
Phân của người bệnh
4. Phiếu xét nghiệm
Điền đầy đủ thông tin theo mẫu yêu cầu
III. CÁC BƯỚC TIẾN HÀNH
Các bước tiến hành thực hiện theo phương tiện, hóa chất được ví dụ ở
trên.
1. Lấy bệnh phẩm
Theo đúng quy định của chuyên ngành Vi sinh (Xem Phụ lục 1).
2. Tiến hành kỹ thuật
Chuẩn bị tiêu bản
Nhuộm Cholerae DFA (direct fluorescent antibody)
- Phủ dung dịch nhuộm huỳnh quang lên tiêu bản, để 2 phút
- Rửa lại bằng nước để loại bỏ huỳnh quang thừa rồi để khô, soi dưới kính hiển vi huỳnh
IV. NHẬN ĐỊNH KẾT QUẢ
Vibrio cholerae có hình ảnh phẩy khuẩn, bắt màu vàng xanh trên nền tím đen dưới kính hiển vi huỳnh quang.
V. NHỮNG SAI SÓT VÀ XỬ TRÍ
Có thể gây âm tính giả nếu số lượng vi khuẩn quá ít.
Chlamydia test nhanh
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đích
Xác định nhanh Chlamydia có trong bệnh phẩm.
2. Nguyên lý
Sử dụng kháng thể đặc hiệu kháng lại lipopolysacchride (LPS) của vi khuẩn Chlamydia trachomatis để phát hiện sự có mặt của Chlamydia trachomatis trong bệnh phẩm.
II. CHUẨN BỊ
1. Người thực hiện
- Người thực hiện Cán bộ xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành Vi
- Người nhận định và phê duyệt kết quả: Cán bộ xét nghiệm có trình độ đại học hoặc sau đại học về chuyên ngành Vi
2. Phương tiện, hóa chất
Phương tiện, hóa chất như ví dụ dưới đây hoặc tương đương.
Trang thiết bị
- Bàn phụ khoa
- Tủ an toàn sinh học cấp 2
- Đèn phụ khoa
Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
| STT | Chi phí hóa chất, vật tư tiêu hao | Đơn vị | Số lượng |
| 1 | Bộ Kit làm xét nghiệm | test | 1,000 |
| 2 | Micropipette 50 – 200 µl | cái | 1,000 |
| 3 | Đầu côn 200 µl | cái | 3,000 |
| 4 | Bông | Kg | 0,001 |
| 5 | Cồn 90 độ (vệ sinh dụng cụ) | ml | 10,000 |
| 6 | Đèn cồn | Cái | 1,000 |
| 7 | Panh | Cái | 1,000 |
| 8 | Mỏ vịt (to, vừa và nhỏ) | Cái | 1,000 |
| 9 | Thùng đựng dung dịch khử khuẩn ngâm mỏ vịt | ||
| 10 | Khay đựng bệnh phẩm | Cái | 1,000 |
| 11 | Hộp vận chuyển bệnh phẩm | Cái | 1,000 |
| 12 | Mũ | Cái | 1,000 |
| 13 | Khẩu trang | Cái | 1,000 |
| 14 | Găng tay | Đôi | 2,000 |
| 15 | Găng tay xử lý dụng cụ | Đôi | 2,000 |
| 16 | Quần áo bảo hộ | Bộ | 1,000 |
| 17 | Ống nghiệm thủy tinh | Ống | 1,000 |
| 18 | Bút viết kính | Cái | 1,000 |
| 19 | Bút bi | Cái | 1,000 |
| 20 | Bật lửa | Cái | 1,000 |
| 21 | Sổ lưu kết quả xét nghiệm | Tờ | 1,000 |
| 22 | Cồn sát trùng tay nhanh | ml | 2,000 |
| 23 | Dung dịch nước rửa tay | ml | 8,000 |
| 24 | Khăn lau tay | Cái | 1,000 |
| 25 | Giấy trả kết quả xét nghiệm | Tờ | 2,000 |
3. Bệnh phẩm
Dịch, mủ âm đạo, mủ niệu đạo
4. Phiếu xét nghiệm
Điền đầy đủ thông tin theo mẫu yêu cầu
III. CÁC BƯỚC TIẾN HÀNH
Các bước tiến hành thực hiện theo phương tiện, hóa chất được ví dụ ở trên.
1. Lấy bệnh phẩm
Theo đúng quy định của chuyên ngành Vi sinh (Xem Phụ lục 1).
2. Tiến hành kỹ thuật
Bỏ thanh thử ra khỏi túi bảo quản
Xoay tăm bông bệnh phẩm trong lọ, tách chiết tế bào 3 – 4 lần, bỏ tăm bông ra
Sử dụng micropipette hút 150µl dung dịch bệnh phẩm nhỏ vào thanh thử.
Để thanh thử ở nhiệt độ phòng. Đọc kết quả sau 20 phút
IV. NHẬN ĐỊNH KẾT QUẢ
Trên thanh thử xuất hiện 2 vạch màu tím đỏ: C là vạch kiểm tra (Control line), T là vạch thử nghiệm (Test line) hoặc chỉ có 1 vạch
Ghi kết quả như bảng sau:
| Hiện tượng | Kết quả |
| Trên thanh thử xuất hiện 2 vạch màu tím đỏ | Dương tính |
| Trên thanh thử xuất hiện 1 vạch (kiểm tra C) | Âm tính |
| Trên thanh thử không xuất hiện vạch C | Test hỏng |
Lưu ý: Bệnh phẩm chưa cho vào dung dịch tách chiết tế bào có thể giữ ở nhiệt độ phòng 24h và 72h ở tủ lạnh 2 – 8 độ C
V. NHỮNG SAI SÓT VÀ XỬ TRÍ
- Dịch nhầy ở niệu đạo (nam giới) và ở cổ tử cung (nữ giới) cần được lau sạch để tránh cho kết quả dương tính giả.
- Bệnh phẩm để trong ống nghiệm khô có thể bảo quản trong tủ lạnh (2-80
- C) lâu nhất là 72h. Không được bảo quản trong ngăn đá.
- Phải làm lại mẫu xét nghiệm mới khi thanh thử bị hỏng (thanh thử không xuất hiện vạch tím tại vạch C).
Chlamydia nhuộm huỳnh quang
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đích
Phát hiện nhanh sự có mặt của Chlamydia trong bệnh phẩm.
2. Nguyên lý
Phát hiện các tiểu thể Chlamydia có trong bệnh phẩm bằng phương pháp nhuộm soi trên kính hiển vi huỳnh quang, các tiểu thể Chlamydia được phát sáng trên nền tối.
II. CHUẨN BỊ
1. Người thực hiện
- Người thực hiện Cán bộ xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành Vi
- Người nhận định và phê duyệt kết quả: Cán bộ xét nghiệm có trình độ đại học hoặc sau đại học về chuyên ngành Vi
2. Phương tiện, hóa chất
Phương tiện, hóa chất như ví dụ dưới đây hoặc tương đương.
Trang thiết bị
- Tủ an toàn sinh học cấp 2
- Kính hiển vi huỳnh quang đèn LED
- Thiết bị sấy lam (nếu có)
Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
| STT | Chi phí hóa chất, vật tư tiêu hao | Đơn vị | Số lượng |
| 1 | FAST Auramin O stain | ml | 1,300 |
| 2 | FAST Decolorizer | ml | 1,200 |
| 3 | Cồn 96 độ (vệ sinh dụng cụ và ngâm lam) | ml | 20,000 |
| 4 | Dung dịch khử khuẩn ngâm que phết đờm | ml | 15,000 |
| 5 | Cồn sát trùng tay nhanh | ml | 2,000 |
| 6 | Dung dịch nước rửa tay | ml | 8,000 |
| 7 | Lọ/cốc/ tuýp lấy bệnh phẩm | Lọ | 1,200 |
| 8 | Lam kính | Cái | 1,500 |
| 9 | Lam kính (kiểm chuẩn) | Cái | 0,200 |
| 10 | Que phết đờm | Cái | 1,500 |
| 11 | Giấy lau kính | Tờ | 2,000 |
| 12 | Bông | Kg | 0,001 |
| 13 | Panh | Cái | 0,0001 |
| 14 | Khay đựng bệnh phẩm | Cái | 0,0001 |
| 15 | Hộp vận chuyển bệnh phẩm | Cái | 0,0001 |
| 16 | Hộp lưu tiêu bản | Cái | 0,0001 |
| 17 | Bô can (bình chứa) vật nhiễm | Cái | 0,0001 |
| 18 | Mũ | Cái | 0,020 |
| 19 | Khẩu trang | Cái | 0,020 |
| 20 | Găng tay | Đôi | 2,000 |
| 21 | Găng tay xử lý dụng cụ | Đôi | 0,020 |
| 22 | Quần áo bảo hộ | Bộ | 0,001 |
| 23 | Khăn lau tay | Cái | 0,030 |
| 24 | Túi chứa rác thải lây nhiễm | Cái | 0,0001 |
| 25 | Khăn giấy vệ sinh các bàn làm việc | Tờ | 2,000 |
| 26 | Bút viết kính | Cái | 0,020 |
| 27 | Bút bi | Cái | 0,010 |
| 28 | Sổ nhận bệnh phẩm | Tờ | 0,001 |
| 29 | Sổ lưu kết quả xét nghiệm | Tờ | 0,001 |
| 30 | Sổ bàn giao kết quả xét nghiệm | Tờ | 0,001 |
| 31 | Giấy trả kết quả xét nghiệm | Tờ | 2,000 |
| 32 | Nhãn mã vạch | Cái | 3,000 |
| 33 | QC (nếu thực hiện) * | 0,1 | |
| 34 | EQAS (nếu thực hiện) * | 0,005 |
* Ghi chú:
- Chi phí nội kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình nội kiểm (QC) là 1/10 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lượng ≥ 10 mẫu cho 1 lần tiến hành kỹ thuật).
- Chi phí ngoại kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình ngoại kiểm (EQAS) là 1/200 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lần ngoại kiểm trung bình 2 lần/1 năm).
3. Bệnh phẩm
Dịch niệu đạo, dịch cổ tử cung, các loại dịch khác. …
4. Phiếu xét nghiệm
Điền đầy đủ thông tin theo mẫu yêu cầu
III. CÁC BƯỚC TIẾN HÀNH
1. Lấy bệnh phẩm
Theo đúng quy định của chuyên ngành Vi sinh (Xem Phụ lục 1 và Phụ lục 6)
2. Tiến hành kỹ thuật
Chuẩn bị tiêu bản
Cố định tiêu bản
Nhuộm màu bằng FAST Auramin O
Tẩy và nhuộm nền bằng FAST Decolorizer
Đọc và đánh giá kết quả trên kính hiển vi huỳnh quang đèn LED
IV. NHẬN ĐỊNH KẾT QUẢ
Quan sát các tiểu thể Chlamydia trachomatis bằng vật kính 40 trên kính huỳnh quang đèn LED. Các tiểu thể Chlamydia trachomatis có hình tròn, bầu dục, riêng lẻ hoặc từng đám. tiểu thể bắt màu vàng sáng phát quang trên nền tối. Đếm số lượng tiểu thể và ghi kết quả như bảng sau:
| Số lượng tiểu thể | Kết quả | Mức độ |
| > 50 tiểu thể/ 1 vi trường (Đọc ít nhất 8 vi trường) | Dương tính | 3 + |
| 5-50 tiểu thể/ 1 vi trường (Đọc ít nhất 20 vi trường) | Dương tính | 2+ |
| 20-199 tiểu thể/ 1 dòng (Đọc ít nhất 1 dòng) | Dương tính | 1 + |
| 1-19 tiểu thể/ 1 dòng | Dương tính | Ghi số lượng cụ thể |
| 0 tiểu thể/ ít nhất 1 dòng | Âm tính |
Lưu ý: 1 dòng lam tương đương 40 vi trường.
V. NHỮNG SAI SÓT VÀ XỬ TRÍ
- Mỗi mẻ nhuộm không nên quá 12 tiêu bản, các tiêu bản để cách nhau ít nhất 1
- Tiểu thể phát quang yếu có thể do tiêu bản sau khi nhuộm không đọc ngay, tiêu bản bị tiếp xúc nhiều với ánh sáng.
- Tiểu thể phát quang yếu có thể do chất lượng hóa chất không đạt do bảo quản chưa đúng, quá hạn.
Virus test nhanh
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đích
Phát hiện kháng nguyên hoặc kháng thể của 1 số loại virus từ bệnh phẩm.
2. Nguyên lý
Dựa trên nguyên lý của kỹ thuật sắc ký miễn dịch.
II. CHUẨN BỊ
1.Người thực hiện
- Người thực hiện: Cán bộ xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành Vi
- Người nhận định và phê duyệt kết quả: Cán bộ xét nghiệm có trình độ đại học hoặc sau đại học về chuyên ngành Vi
2. Phương tiện, hóa chất
Phương tiện, hóa chất như ví dụ dưới đây hoặc tương đương.
Trang thiết bị
- Tủ an toàn sinh học
- Micropipette
- Đồng hồ bấm giây
- Máy ly tâm thường
Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
Định mức sinh phẩm và vật tư tiêu hao cho 10 mẫu/lần thực hiện (VD)
| STT | Chi phí hóa chất, vật tư tiêu hao | Đơn vị | Số lượng |
| 1 | Ống lấy bệnh phẩm | Ống | 1,000 |
| 2 | Bơm tiêm | Cái | 1,000 |
| 3 | Bông | Kg | 0,001 |
| 4 | Cồn 90 độ (vệ sinh dụng cụ) | Ml | 10,000 |
| 5 | Panh | Cái | 0,0001 |
| 6 | Khay đựng bệnh phẩm | Cái | 0,0001 |
| 7 | Hộp vận chuyển bệnh phẩm | Cái | 0,0001 |
| 8 | Hóa chất chính | Test | 1,000 |
| 9 | Khấu hao sinh phẩm cho chạy chứng và kiểm tra chất lượng | Test | 0,200 |
| 10 | Đầu côn vàng | Cái | 2,000 |
| 11 | Axít ngâm rửa | Ml | 10,000 |
| 12 | Ống nghiệm thủy tinh | Ống | 1,000 |
| 13 | Mũ | Cái | 0,020 |
| 14 | Khẩu trang | Cái | 0,020 |
| 15 | Găng tay | Đôi | 2,000 |
| 16 | Găng tay xử lý dụng cụ | Đôi | 0,020 |
| 17 | Quần áo bảo hộ | Bộ | 0,001 |
| 18 | Bút viết kính | Cái | 0,020 |
| 19 | Bút bi | Cái | 0,010 |
| 20 | Sổ lưu kết quả xét nghiệm | Quyển | 0,001 |
| 21 | Cồn sát trùng tay nhanh | Ml | 1,000 |
| 22 | Dung dịch nước rửa tay | Ml | 8,000 |
| 23 | Khăn lau tay | Cái | 0,010 |
| 24 | Giấy trả kết quả xét nghiệm | Tờ | 2,000 |
3.Bệnh phẩm
Huyết thanh hoặc huyết tương của người bệnh
4.Phiếu xét nghiệm
Điền đầy đủ thông tin theo mẫu phiếu yêu cầu
III. CÁC BƯỚC TIẾN HÀNH
Các bước tiến hành thực hiện theo phương tiện, hóa chất được ví dụ ở trên.
1. Lấy bệnh phẩm
- Theo đúng quy định của chuyên ngành Vi sinh (xem phụ lục 2)
- Từ chối những bệnh phẩm không đạt yêu cầu (xem phụ lục 6).
2. Tiến hành kỹ thuật
Ly tâm ống bệnh phẩm
Bóc thanh xét nghiệm và ghi mã số bệnh phẩm tương ứng Thực hiện các bước tiếp theo quy trình hướng dẫn của nhà sản xuất
IV. NHẬN ĐỊNH KẾT QUẢ
Đọc kết quả theo hướng dẫn của nhà sản xuất.
V. NHỮNG SAI SÓT VÀ XỬ TRÍ
- Đọc kết quả trước hoặc sau thời gian qui định có thể làm sai lệch kết quả.
- Cho quá ít bệnh phẩm, hay quá nhiều dung dịch pha loãng có thể làm kết quả khó đọc.
- Tham khảo thêm hướng dẫn của nhà sản xuất
HBsAg test nhanh
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đích
Phát hiện kháng nguyên HBsAg của virus viêm gan B (HBV) trong huyết thanh (huyết tương).
2. Nguyên lý
Dựa trên nguyên lý của kỹ thuật sắc ký miễn dịch.
II. CHUẨN BỊ
1. Người thực hiện
- Người thực hiện Cán bộ xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành Vi
- Người nhận định và phê duyệt kết quả: Cán bộ xét nghiệm có trình độ đại học hoặc sau đại học về chuyên ngành Vi
2. Phương tiện, hóa chất
Phương tiện, hóa chất như ví dụ dưới đây hoặc tương đương.
Trang thiết bị
- Micropipette 50 µl -100 µl.
- Máy ly tâm thường.
- Đồng hồ bấm giây
Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
Định mức sinh phẩm và vật tư tiêu hao cho 10 mẫu/lần thực hiện (VD)
| STT | Chi phí hóa chất, vật tư tiêu hao | Đơn vị | Số lượng |
| 1 | Bông | Kg | 0,001 |
| 2 | Dây garô | Cái | 0,001 |
| 3 | Tube đựng bệnh phẩm | Cái | 1,000 |
| 4 | Sinh phẩm chẩn đoán | Test | 1,000 |
| 5 | Khấu hao sinh phẩm cho kiểm tra chất lượng | Test | 0,200 |
| 6 | Ngoại kiểm (nếu có)* | 0,020 | |
| 7 | Đầu côn 200 µl | Cái | 1,200 |
| 8 | Giấy thấm | Cuộn | 0,100 |
| 9 | Giấy xét nghiệm | Tờ | 2,000 |
| 10 | Sổ lưu kết quả xét nghiệm | Tờ | 0,001 |
| 11 | Bút viết kính | Cái | 0,020 |
| 12 | Bút bi | Cái | 0,010 |
| 13 | Mũ | Cái | 0,020 |
| 14 | Khẩu trang | Cái | 0,020 |
| 15 | Găng tay | Đôi | 0,100 |
| 16 | Găng tay xử lý dụng cụ | Đôi | 0,020 |
| 17 | Quần áo bảo hộ | Bộ | 0,005 |
| 18 | Dung dịch nước rửa tay | Ml | 8,000 |
| 19 | Cồn sát trùng tay nhanh | Ml | 1,000 |
| 20 | Dung dịch khử trùng | Ml | 10,000 |
| 21 | Khăn lau tay | Cái | 0,010 |
* Ghi chú: Chi phí ngoại kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình ngoại kiểm (EQAS) là 1/50 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lần ngoại kiểm trung bình 2 lần/1 năm).
3. Bệnh phẩm
Huyết thanh hoặc huyết tương của người bệnh.
4. Phiếu xét nghiệm
Điền đầy đủ thông tin theo mẫu phiếu yêu cầu.
III. CÁC BƯỚC TIẾN HÀNH
Các bước tiến hành thực hiện theo phương tiện, hóa chất được ví dụ ở trên.
1. Lấy bệnh phẩm
- Theo đúng quy định của chuyên ngành Vi sinh (xem phụ lục 2)
- Từ chối những bệnh phẩm không đạt yêu cầu (xem phụ lục 6).
2. Tiến hành kỹ thuật
Bộ sinh phẩm Determine (VD).
| Các bước | Xét nghiệm phát hiện HBsAg nhanh |
| 1 | Tách rời từng thanh xét nghiệm rồi bóc vỏ Ghi mã bệnh phẩm tương ứng |
| 2 | Nhỏ 50 µl huyết thanh hoặc huyết tương vào vùng nhỏ bệnh phẩm |
| 3 | Chờ 15 phút đọc kết quả |
IV. NHẬN ĐỊNH KẾT QUẢ
- Dương tính: Xuất hiện 2 vạch đỏ ở phần chứng và phần bệnh phẩm.
- Âm tính: Chỉ có 1 vạch đỏ ở phần chứng.
- Không xác định:
+ Chỉ có 1 vạch đỏ ở phần bệnh phẩm.
+ Không có vạch đỏ nào xuất hiện ở phần chứng và phần bệnh phẩm.
V. NHỮNG SAI SÓT VÀ XỬ TRÍ
- Thời gian đọc kết quả à ghi lại thời gian làm xét nghiệm và thời gian đọc kết quả để tránh dương tính giả và âm tính giả.
- Chất lượng bệnh phẩm: những mẫu bệnh phẩm tan huyết sẽ ảnh hưởng đến chất lượng và kết quả xét nghiệm.
HIV Ab test nhanh
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đích
Phát hiện kháng thể kháng HIV trong huyết thanh hoặc huyết tương.
2. Nguyên lý
Phát hiện kháng thể kháng HIV dựa trên nguyên lý của kỹ thuật sắc ký miễn dịch.
II. CHUẨN BỊ
1. Người thực hiện
- Người thực hiện: Cán bộ xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành Vi sinh đồng thời được đào tạo và có chứng chỉ về xét nghiệm HIV theo qui định của Bộ Y tế.
- Người nhận định và phê duyệt kết quả: Cán bộ xét nghiệm có trình độ đại học hoặc sau đại học về chuyên ngành Vi sinh đồng thời được đào tạo và có chứng chỉ về xét nghiệm HIV theo qui định của Bộ Y tế.
2. Phương tiện, hóa chất
Phương tiện, hóa chất như ví dụ dưới đây hoặc tương đương.
Trang thiết bị
- Máy ly tâm thường.
- Micropipette 50 µl -100 µl.
- Đồng hồ bấm giây
Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
Thực hiện xét nghiệm 01 mẫu/lần.
| STT | Chi phí hóa chất, vật tư tiêu hao | Đơn vị | Số lượng |
| 1 | Bông | Kg | 0,001 |
| 2 | Dây garô | Cái | 0,001 |
| 3 | Cồn | ml | 1,000 |
| 4 | Bơm kim tiêm | Cái | 1,000 |
| 5 | Panh | Cái | 0,0001 |
| 6 | Khay đựng bệnh phẩm | Cái | 0,0001 |
| 7 | Hộp vận chuyển bệnh phẩm | Cái | 0,001 |
| 8 | Tube đựng bệnh phẩm | Cái | 1,000 |
| 9 | Sinh phẩm chẩn đoán | Test | 1,000 |
| 10 | Khấu hao sinh phẩm cho chạy chứng | Test | 0,200 |
| 11 | EQAS (nếu thực hiện) * | 0,02 | |
| 12 | Đầu côn 200 µl | Cái | 2,000 |
| 13 | Giấy thấm | Cuộn | 0,100 |
| 14 | Giấy xét nghiệm | Tờ | 2,000 |
| 15 | Sổ lưu kết quả xét nghiệm | Tờ | 0,001 |
| 16 | Bút viết kính | Cái | 0,020 |
| 17 | Bút bi | Cái | 0,010 |
| 18 | Mũ | Cái | 0,020 |
| 19 | Khẩu trang | Cái | 0,020 |
| 20 | Găng tay | Đôi | 0,100 |
| 21 | Găng tay xử lý dụng cụ | Đôi | 0,020 |
| 22 | Quần áo bảo hộ | Bộ | 0,005 |
| 23 | Dung dịch nước rửa tay | ml | 8,000 |
| 24 | Cồn sát trùng tay nhanh | ml | 1,000 |
| 25 | Dung dịch khử trùng | ml | 10,000 |
| 26 | Khăn lau tay | Cái | 0,010 |
* Ghi chú: Chi phí ngoại kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình ngoại kiểm (EQAS) là 1/50 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lần ngoại kiểm trung bình 2 lần/1 năm).
3. Bệnh phẩm
Huyết thanh, huyết tương của người bệnh
4. Phiếu xét nghiệm
Điền đầy đủ thông tin theo mẫu phiếu yêu cầu
III. CÁC BƯỚC TIẾN HÀNH
Các bước tiến hành thực hiện theo phương tiện, hóa chất được ví dụ ở trên.
1. Lấy bệnh phẩm
- Theo đúng quy định của chuyên ngành Vi sinh: xem chi tiết phụ lục 2
- Từ chối những bệnh phẩm không đạt yêu cầu: xem chi tiết phụ lục
2. Tiến hành kỹ thuật
Bộ sinh phẩm Determine HIV ½ Ab.(VD).
| Các bước | Xét nghiệm phát hiện kháng thể HIV nhanh |
| 1 | Tách rời từng thanh xét nghiệm rồi bóc vỏ Ghi mã bệnh phẩm xét nghiệm tương ứng |
| 2 | Nhỏ 50 µl huyết thanh, huyết tương hoặc máu toàn phần vào vùng nhỏ bệnh phẩm |
| 3 | Chờ 15 phút đọc kết quả |
IV. NHẬN ĐỊNH KẾT QUẢ (Kết quả sơ bộ)
- Dương tính: Xuất hiện 2 vạch đỏ ở phần chứng và phần bệnh phẩm.
- Âm tính: Chỉ có 1 vạch đỏ ở phần chứng.
- Không xác định:
+ Chỉ có 1 vạch đỏ ở phần bệnh phẩm.
+ Không có vạch đỏ nào xuất hiện ở phần chứng và phần bệnh phẩm.
V. NHỮNG SAI SÓT VÀ XỬ TRÍ
- Thời gian đọc KQ à ghi lại thời gian làm xét nghiệm và thời gian đọc kết quả để tránh dương tính giả và âm tính giả.
- Chất lượng bệnh phẩm: những mẫu bệnh phẩm tan huyết sẽ ảnh hưởng đến chất lượng và kết quả xét nghiệm.
HIV Ag/Ab test nhanh
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đích
Phát hiện kháng nguyên p24 và kháng thể kháng HIV-1 và HIV-2 trong huyết thanh hoặc huyết tương.
2. Nguyên lý
Phát hiện kháng nguyên p24 và kháng thể kháng HIV-1 và HIV-2 dựa trên nguyên lý của kỹ thuật sắc ký miễn dịch.
II. CHUẨN BỊ
1. Người thực hiện
– Người thực hiện: Cán bộ xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành Vi sinh đồng thời được đào tạo và có chứng chỉ về xét nghiệm HIV theo qui định của Bộ Y tế.
– Người nhận định và phê duyệt kết quả: Cán bộ xét nghiệm có trình độ đại học hoặc sau đại học về chuyên ngành Vi sinh đồng thời được đào tạo và có chứng chỉ về xét nghiệm HIV theo qui định của Bộ Y tế.
2. Phương tiện, hóa chất
Phương tiện, hóa chất như ví dụ dưới đây hoặc tương đương.
Trang thiết bị
- Micropipette 50 µl – 100 µl.
- Máy ly tâm thường.
- Đồng hồ bấm giây.
Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
Thực hiện xét nghiệm 01 mẫu/lần.
| STT | Chi phí hóa chất, vật tư tiêu hao | Đơn vị | Số lượng |
| 1 | Bông | Kg | 0,001 |
| 2 | Dây garô | Cái | 0,001 |
| 3 | Cồn | ml | 1,000 |
| 4 | Bơm kim tiêm | Cái | 1,000 |
| 5 | Panh | Cái | 0,0001 |
| 6 | Khay đựng bệnh phẩm | Cái | 0,0001 |
| 7 | Hộp vận chuyển bệnh phẩm | Cái | 0,001 |
| 8 | Tube đựng bệnh phẩm | Cái | 1,000 |
| 9 | Sinh phẩm chẩn đoán | Test | 1,000 |
| 10 | Khấu hao sinh phẩm cho chạy chứng và kiểm tra chất lượng | Test | 0,200 |
| 11 | EQAS (nếu thực hiện) * | 0,02 | |
| 12 | Đầu côn 200 µl | Cái | 2,000 |
| 13 | Giấy thấm | Cuộn | 0,100 |
| 14 | Giấy xét nghiệm | Tờ | 2,000 |
| 15 | Sổ lưu kết quả xét nghiệm | Tờ | 0,001 |
| 16 | Bút viết kính | Cái | 0,020 |
| 17 | Bút bi | Cái | 0,010 |
| 18 | Mũ | Cái | 0,020 |
| 19 | Khẩu trang | Cái | 0,020 |
| 20 | Găng tay | Đôi | 0,100 |
| 21 | Găng tay xử lý dụng cụ | Đôi | 0,020 |
| 22 | Quần áo bảo hộ | Bộ | 0,005 |
| 23 | Dung dịch nước rửa tay | ml | 8,000 |
| 24 | Cồn sát trùng tay nhanh | ml | 1,000 |
| 25 | Dung dịch khử trùng | ml | 10,000 |
| 26 | Khăn lau tay | Cái | 0,010 |
* Ghi chú: Chi phí ngoại kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình ngoại kiểm (EQAS) là 1/50 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lần ngoại kiểm trung bình 2 lần/1 năm).
3. Bệnh phẩm
Huyết thanh, huyết tương hoặc máu toàn phần của người bệnh
4. Phiếu xét nghiệm
Điền đầy đủ thông tin theo mẫu phiếu yêu cầu
III. CÁC BƯỚC TIẾN HÀNH
Các bước tiến hành thực hiện theo phương tiện, hóa chất được ví dụ ở trên.
1. Lấy bệnh phẩm
- Theo đúng quy định của chuyên ngành Vi sinh: xem chi tiết phụ lục 2
- Từ chối những bệnh phẩm không đạt yêu cầu: xem chi tiết phụ lục
2. Tiến hành kỹ thuật
Bộ sinh phẩm Alere Determine HIV ½ Ag/Ab Combo – Alere (VD)
| Các bước | Xét nghiệm phát hiện kháng nguyên-kháng thể HIV |
| Đối với huyết thanh/huyết tương | |
| 1 | Tách rời từng thanh xét nghiệm rồi xé bao bảo vệ thanh xét nghiệm. Ghi mã bệnh phẩm xét nghiệm tương ứng |
| 2 | Nhỏ 50 µl huyết thanh hoặc huyết tương vào vùng nhỏ bệnh phẩm |
| 3 | Chờ 20 phút đọc kết quả |
| Đối với máu toàn phần | |
| 1 | Tách rời từng thanh xét nghiệm rồi bóc vỏ |
| Ghi mã bệnh phẩm xét nghiệm tương ứng | |
| 2 | Nhỏ 50 µl huyết thanh hoặc huyết tương vào vùng nhỏ bệnh phẩm |
| 3 | Đợi một phút, sau đó cho một giọt dung dịch đệm Chase vào vùng nhỏ mẫu bệnh phẩm |
| 4 | Chờ 20 phút đọc kết quả |
| Lưu ý (đối với cả huyết thanh, huyết tương và máu toàn phần): Không đọc kết quả sau quá 30 phút | |
IV. NHẬN ĐỊNH KẾT QUẢ
1. Điều kiện của phản ứng:
- Vạch chứng phải chuyển màu đỏ khi xét nghiệm hoàn tất.
- Nếu vạch chứng không xuất hiện thì kết quả xét nghiệm không có giá trị và mẫu phẩm cần phải được thử lại.
2. Nhận định kết quả
- Có phản ứng với kháng thể: Xuất hiện 2 vạch đỏ ở vùng chứng và vùng kháng thể.
- Có phản ứng với kháng nguyên (p24): Xuất hiện 2 vạch đỏ ở vùng chứng và vùng kháng nguyên.
- Có phản ứng với kháng thể và kháng nguyên (p24): Xuất hiện 3 vạch đỏ ở vùng chứng, vùng kháng thể và vùng kháng nguyên.
- Âm tính: Chỉ có 1 vạch đỏ ở phần chứng.
- Không xác định:
+ Chỉ có 1 vạch đỏ ở phần bệnh phẩm.
+ Không có vạch đỏ nào xuất hiện ở phần chứng và phần bệnh phẩm ®
cần phải thử lại mẫu phẩm.
V. NHỮNG SAI SÓT VÀ XỬ TRÍ
Đọc kết quả sau quá 30 phút dễ gây phản ứng dương tính giả ” Nên có đồng hồ đặt giờ để đọc kết quả đúng giờ qui định.
Dengue virus NS1Ag test nhanh
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đích
Phát hiện kháng nguyên NS1 của virus dengue trong huyết thanh hoặc huyết tương.
2. Nguyên lý
Phát hiện kháng nguyên NS1 của virus dengue dựa trên nguyên lý của kỹ thuật sắc ký miễn dịch.
II. CHUẨN BỊ
1. Người thực hiện
- Người thực hiện Cán bộ xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành Vi
- Người nhận định và phê duyệt kết quả: Cán bộ xét nghiệm có trình độ đại học hoặc sau đại học về chuyên ngành Vi
2. Phương tiện, hóa chất
Phương tiện, hóa chất như ví dụ dưới đây hoặc tương đương.
| 1 | Ghi mã bệnh phẩm xét nghiệm tương ứng |
| 2 | Nhỏ 50 µl huyết thanh hoặc huyết tương vào vùng nhỏ bệnh phẩm |
| 3 | Đợi một phút, sau đó cho một giọt dung dịch đệm Chase vào vùng nhỏ mẫu bệnh phẩm |
| 4 | Chờ 20 phút đọc kết quả |
| Lưu ý (đối với cả huyết thanh, huyết tương và máu toàn phần): Không đọc kết quả sau quá 30 phút | |
- Máy ly tâm thường
- Pipet vi lượng 5 µl đến 100 µl.
- Đồng hồ bấm giây.
Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
Thực hiện xét nghiệm 01 mẫu/lần.
| STT | Chi phí hóa chất, vật tư tiêu hao | Đơn vị | Số lượng |
| 1 | Bông | Kg | 0,001 |
| 2 | Dây garô | Cái | 0,001 |
| 3 | Cồn | ml | 1,000 |
| 4 | Bơm kim tiêm | Cái | 1,000 |
| 5 | Panh | Cái | 0,0001 |
| 6 | Khay đựng bệnh phẩm | Cái | 0,0001 |
| 7 | Hộp vận chuyển bệnh phẩm | Test | 0,001 |
| 8 | Tube đựng bệnh phẩm | Cái | 1,000 |
| 9 | Sinh phẩm chẩn đoán | Test | 1,000 |
| 10 | Khấu hao sinh phẩm cho kiểm tra chất lượng | Test | 0,200 |
| 11 | Đầu côn 200 µl | Cái | 2,000 |
| 12 | Giấy thấm | Cuộn | 0,100 |
| 13 | Giấy xét nghiệm | Tờ | 2,000 |
| 14 | Sổ lưu kết quả xét nghiệm | Tờ | 0,001 |
| 15 | Bút viết kính | Cái | 0,020 |
| 16 | Bút bi | Cái | 0,010 |
| 17 | Mũ | Cái | 0,020 |
| 18 | Khẩu trang | Cái | 0,020 |
| 19 | Găng tay | Đôi | 0,100 |
| 20 | Găng tay xử lý dụng cụ | Đôi | 0,020 |
| 21 | Quần áo bảo hộ | Bộ | 0,005 |
| 22 | Dung dịch nước rửa tay | ml | 8,000 |
| 23 | Cồn sát trùng tay nhanh | ml | 1,000 |
| 24 | Dung dịch khử trùng | ml | 10,000 |
| 25 | Khăn lau tay | Cái | 0,010 |
3. Bệnh phẩm
Huyết thanh hoặc huyết tương
4. Phiếu xét nghiệm
Điền đầy đủ thông tin theo mẫu yêu cầu
III. CÁC BƯỚC TIẾN HÀNH
Các bước tiến hành thực hiện theo phương tiện, hóa chất được ví dụ ở trên.
1. Lấy bệnh phẩm
- Theo đúng quy định của chuyên ngành Vi sinh: xem chi tiết phụ lục
- Từ chối những bệnh phẩm không đạt yêu cầu: xem chi tiết phụ lục
2.Tiến hành kỹ thuật
Bộ sinh phẩm Dengue NS1Ag Strip – BioRad (VD)
| Các bước | Xét nghiệm định tính Dengue NS1 Ag |
| 2.1 | Để Số lượng sinh phẩm cần dùng ở nhiệt độ phòng 30 phút trước khi làm xét nghiệm |
| 2.2 | Sử dụng ống nghiệm bằng nhựa hoặc thủy tinh có chiều cao > 45 mm và đường kính nhỏ hơn 15 mm. Ghi số bệnh phẩm lên ống nghiệm. |
| 2.3 | Hút huyết thanh/huyết tương vào trong ống nghiệm. |
| 2.4 | Nhỏ thêm 1 giọt dung dịch di chuyển (migration buffer) vào ống nghiệm. Lắc nhẹ nhàng để trộn đều. |
| 2.5 | Đặt thanh thử theo phương thẳng đứng vào trong ống nghiệm, hướng chiều mũi tên xuống dưới. Kiểm tra để đảm bảo thanh thử đã được nhúng vào dung dịch bệnh phẩm đã pha loãng. |
| 2.6 | Đọc kết quả sau 15 phút |
IV. NHẬN ĐỊNH KẾT QUẢ
- Âm tính: Chỉ 1 một đường màu xuất hiện ở vùng chứng.
- Dương tính: 2 đường màu xuất hiện ở vùng chứng và vùng thử nghiệm
- Không có giá trị: Không thấy xuất hiện đường màu nào. Phải tiến hành làm lại xét nghiệm với một thanh thử khác.
Lưu ý: Đối với những mẫu huyết thanh/huyết tương kép và những mẫu âm tính thì để nguyên thanh thử trong ống nghiệm và đọc lại kết quả sau 15 phút nữa.
V. NHỮNG SAI SÓT VÀ XỬ TRÍ
Không thấy sự di chuyển của bệnh phẩm trên màng sắc ký ® Kiểm tra để đảm bảo thanh thử đã được nhúng vào dung dịch bệnh phẩm đã pha loãng.
Dengue virus NS1Ag/IgM/IgG test nhanh
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đích
Phát hiện kháng nguyên NS1 và kháng thể IgM/IgG kháng virus dengue trong huyết thanh, huyết tương hoặc máu toàn phần..
2. Nguyên lý
Phát hiện kháng nguyên NS1 của virus dengue và kháng thể IgM/IgG kháng virus dengue dựa trên nguyên lý của kỹ thuật sắc ký miễn dịch.
II. CHUẨN BỊ
1. Người thực hiện
- Người thực hiện: Cán bộ xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành Vi
- Người nhận định và phê duyệt kết quả: Cán bộ xét nghiệm có trình độ đại học hoặc sau đại học về chuyên ngành Vi
2. Phương tiện, hóa chất
Phương tiện, hóa chất như ví dụ dưới đây hoặc tương đương.
Trang thiết bị
- Máy ly tâm thường
- Micropipette 5 µl đến 100 µl.
- Đồng hồ bấm giây
Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
Thực hiện xét nghiệm 01 mẫu/lần.
| TT | Chi phí hóa chất, vật tư tiêu hao | Đơn vị | Số lượng |
| 1 | Bông | Kg | 0,001 |
| 2 | Dây garô | Cái | 0,001 |
| 3 | Cồn | ml | 1,000 |
| 4 | Bơm kim tiêm | Cái | 1,000 |
| 5 | Panh | Cái | 0,0001 |
| 6 | Khay đựng bệnh phẩm | Cái | 0,0001 |
| 7 | Hộp vận chuyển bệnh phẩm | Test | 0,001 |
| 8 | Tube đựng bệnh phẩm | Cái | 1,000 |
| 9 | Sinh phẩm chẩn đoán | Test | 1,000 |
| 10 | Khấu hao sinh phẩm cho kiểm tra chất lượng | Test | 0,300 |
| 11 | Đầu côn 200 µl | Cái | 2,000 |
| 12 | Giấy thấm | Cuộn | 0,100 |
| 13 | Giấy xét nghiệm | Tờ | 2,000 |
| 14 | Sổ lưu kết quả xét nghiệm | Tờ | 0,001 |
| 15 | Bút viết kính | Cái | 0,020 |
| 16 | Bút bi | Cái | 0,010 |
| 17 | Mũ | Cái | 0,020 |
| 18 | Khẩu trang | Cái | 0,020 |
| 19 | Găng tay | Đôi | 0,100 |
| 20 | Găng tay xử lý dụng cụ | Đôi | 0,020 |
| 21 | Quần áo bảo hộ | Bộ | 0,005 |
| 22 | Dung dịch nước rửa tay | ml | 8,000 |
| 23 | Cồn sát trùng tay nhanh | ml | 1,000 |
| 24 | Dung dịch khử trùng | ml | 10,000 |
| 25 | Khăn lau tay | Cái | 0,010 |
3. Bệnh phẩm
Huyết thanh, huyết tương hoặc máu toàn phần
4. Phiếu xét nghiệm
Điền đầy đủ thông tin theo mẫu yêu cầu
III. CÁC BƯỚC TIẾN HÀNH
Các bước tiến hành thực hiện theo phương tiện, hóa chất được ví dụ ở trên.
1. Lấy bệnh phẩm
- Theo đúng quy định của chuyên ngành Vi sinh: xem chi tiết phụ lục
- Từ chối những bệnh phẩm không đạt yêu cầu: xem chi tiết phụ lục
- Tiến hành kỹ thuật:Bộ sinh phẩm SD Bioline Dengue Duo – SD (VD)
| Các bước | Xét nghiệm định tính Dengue NS1 Ag & Dengue IgM/IgG |
| 2.1 | Để Số lượng sinh phẩm cần dùng ở nhiệt độ phòng 30 phút trước khi làm xét nghiệm |
| 2.2 | Bóc vỏ nhôm lấy thanh thử đặt lên bề mặt phẳng |
| Dengue NS1 Ag | |
| 2.3 | Dùng pipet nhựa to có sẵn trong hộp nhỏ 3 giọt (tương đương 100 ml) bệnh phẩm vào giếng nhỏ bệnh phẩm (S) |
| 2.4 | Đọc kết quả sau 15 phút – 20 phút |
| Dengue IgM/IgG | |
| 2.5 | Dùng pipet nhựa nhỏ có sẵn trong hộp hút huyết thanh/huyết tương đến vạch màu xanh (tương đương 10 ml), nhỏ bệnh phẩm vào giếng nhỏ bệnh phẩm (S) |
| 2.6 | Nhỏ 4 giọt dung dịch pha loãng vào giếng hình tròn ở phần đầu của thanh thử |
| 2.7 | Đọc kết quả sau 15 phút – 20 phút |
IV. NHẬN ĐỊNH KẾT QUẢ
1. Dengue NS1 Ag
- Âm tính: Chỉ 1 một đường màu xuất hiện ở vùng chứng.
- Dương tính: 2 đường màu xuất hiện ở vùng chứng và vùng thử nghiệm.
- Không có giá trị: Không thấy xuất hiện đường màu nào. Phải tiến hành làm lại xét nghiệm với một thanh thử khác.
2. Dengue IgM/IgG
Việc đánh giá kết quả cần dựa vào kết quả phối hợp của vạch thử nghiệm IgM, IgG và vạch chứng.
* Nhiễm trùng tiên phát
Vạch màu hồng xuất hiện ở vùng IgM và vùng chứng ” Thử nghiệm dương tính với kháng thể IgM và gợi ý tới một nhiễm trùng dengue tiên phát.
* Nhiễm trùng thứ phát
- Vạch mầu hồng xuất hiện ở vùng IgM, IgG và vùng chứng ” Kháng thể IgM và IgG dương tính và gợi ý tới một nhiễm trùng dengue thứ phát.
- Vạch mầu hồng xuất hiện ở vùng IgG và vùng chứng ” Kháng thể IgG dương tính và gợi ý tới một nhiễm trùng dengue thứ phát.
* Âm tính
Vạch mầu hồng chỉ xuất hiện ở vùng chứng ” Không phát hiện được kháng thể IgM và IgG kháng dengue. Kiểm tra lại sau 3 – 4 ngày nếu nghi ngờ có nhiễm virus dengue.
V. NHỮNG SAI SÓT VÀ XỬ TRÍ
Đọc kết quả sau quá 20 phút dễ gây phản ứng dương tính giả “Nên có đồng hồ đặt giờ để đọc kết quả đúng giờ qui định.
Dengue virus IgM/IgG test nhanh
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đích
Phát hiện kháng thể IgM/IgG kháng virus dengue trong huyết thanh, huyết tương hoặc máu toàn phần.
2. Nguyên lý
Phát hiện kháng thể IgM/IgG kháng virus dengue dựa trên nguyên lý của kỹ thuật sắc ký miễn dịch.
II. CHUẨN BỊ
1.Người thực hiện
- Người thực hiện: Cán bộ xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành Vi
- Người nhận định và phê duyệt kết quả: Cán bộ xét nghiệm có trình độ đại học hoặc sau đại học về chuyên ngành Vi
2. Phương tiện, hóa chất
Phương tiện, hóa chất như ví dụ dưới đây hoặc tương đương.
Trang thiết bị
- Máy ly tâm thường
- Micropipette 5 µl đến 100 µl.
- Đồng hồ bấm giây
Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
Thực hiện xét nghiệm 01 mẫu/lần.
| STT | Chi phí hóa chất, vật tư tiêu hao | Đơn vị | Số lượng |
| 1 | Bông | Kg | 0,001 |
| 2 | Dây garô | Cái | 0,001 |
| 3 | Cồn | ml | 1,000 |
| 4 | Bơm kim tiêm | Cái | 1,000 |
| 5 | Panh | Cái | 0,0001 |
| 6 | Khay đựng bệnh phẩm | Cái | 0,0001 |
| 7 | Hộp vận chuyển bệnh phẩm | Test | 0,001 |
| 8 | Tube đựng bệnh phẩm | Cái | 1,000 |
| 9 | Sinh phẩm chẩn đoán | Test | 1,000 |
| 10 | Khấu hao sinh phẩm cho kiểm tra chất lượng | Test | 0,300 |
| 11 | Đầu côn 200 µl | Cái | 2,000 |
| 12 | Giấy thấm | Cuộn | 0,100 |
| 13 | Giấy xét nghiệm | Tờ | 2,000 |
| 14 | Sổ lưu kết quả xét nghiệm | Tờ | 0,001 |
| 15 | Bút viết kính | Cái | 0,020 |
| 16 | Bút bi | Cái | 0,010 |
| 17 | Mũ | Cái | 0,020 |
| 18 | Khẩu trang | Cái | 0,020 |
| 19 | Găng tay | Đôi | 0,100 |
| 20 | Găng tay xử lý dụng cụ | Đôi | 0,020 |
| 21 | Quần áo bảo hộ | Bộ | 0,005 |
| 22 | Dung dịch nước rửa tay | ml | 8,000 |
| 23 | Cồn sát trùng tay nhanh | ml | 1,000 |
| 24 | Dung dịch khử trùng | ml | 10,000 |
| 25 | Khăn lau tay | Cái | 0,010 |
3. Bệnh phẩm
Huyết thanh, huyết tương hoặc máu toàn phần
4. Phiếu xét nghiệm
Điền đầy đủ thông tin theo mẫu yêu cầu
III. CÁC BƯỚC TIẾN HÀNH
Các bước tiến hành thực hiện theo phương tiện, hóa chất được ví dụ ở trên.
1. Lấy bệnh phẩm
- Theo đúng quy định của chuyên ngành Vi sinh: xem chi tiết phụ lục
- Từ chối những bệnh phẩm không đạt yêu cầu: xem chi tiết phụ lục
2. Tiến hành kỹ thuật
Bộ sinh phẩm SD Bioline Dengue Rapid Test – SD (VD)
| Các bước | Xét nghiệm định tính Dengue IgM/IgG |
| 2.1 | Để Số lượng sinh phẩm cần dùng ở nhiệt độ phòng 30 phút trước khi làm xét nghiệm |
| 2.2 | Bóc vỏ nhôm lấy thanh thử đặt lên bề mặt phẳng |
| 2.3 | Nhỏ bệnh phẩm vào giếng nhỏ bệnh phẩm hình tròn (S). Chờ cho huyết thanh thấm hút hết vào phần thấm bệnh phẩm ở giếng tròn. |
| 2.4 | Giữ cho lọ buffer thẳng đứng và cao hơn giếng hình chữ nhật khoảng 1 cm, nhỏ 2 giọt buffer vào giếng hình chữ nhật ở phần đầu của thanh thử. |
| 2.5 | Đọc kết quả sau 15 phút – 20 phút Lưu ý: Mọi kết quả đọc sau quá 20 phút đều không có giá trị và phải thử nghiệm lại. |
IV. NHẬN ĐỊNH KẾT QUẢ
Việc đánh giá kết quả cần dựa vào kết quả phối hợp của vạch thử nghiệm IgM, IgG và vạch chứng.
* Nhiễm trùng tiên phát
Vạch màu hồng xuất hiện ở vùng IgM và vùng chứng ” Thử nghiệm dương tính với kháng thể IgM và gợi ý tới một nhiễm trùng dengue tiên phát.
* Nhiễm trùng thứ phát
- Vạch mầu hồng xuất hiện ở vùng IgM, IgG và vùng chứng ” Kháng thể IgM và IgG dương tính và gợi ý tới một nhiễm trùng dengue thứ phát.
- Vạch mầu hồng xuất hiện ở vùng IgG và vùng chứng ” Kháng thể IgG dương tính và gợi ý tới một nhiễm trùng dengue thứ phát.
* Âm tính
Vạch mầu hồng chỉ xuất hiện ở vùng chứng ” Không phát hiện được kháng thể IgM và IgG kháng dengue. Kiểm tra lại sau 3 – 4 ngày nếu nghi ngờ có nhiễm virus dengue.
* Không có giá trị
Không thấy vạch mầu hồng xuất hiện ở vùng chứng ” Thử nghiệm không có giá trị và cần phải làm lại.
V. NHỮNG SAI SÓT VÀ XỬ TRÍ
Đọc kết quả sau quá 20 phút dễ gây phản ứng dương tính giả “Nên có đồng hồ đặt giờ để đọc kết quả đúng giờ qui định.
Rotavirus test nhanh
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đích
Phát hiện kháng nguyên rota virus trong bệnh phẩm phân.
2. Nguyên lý
Phát hiện kháng nguyên rota virus dựa trên nguyên lý của kỹ thuật sắc ký miễn dịch.
II. CHUẨN BỊ
1. Người thực hiện
- Người thực hiện: Cán bộ xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành Vi
- Người nhận định và phê duyệt kết quả: Cán bộ xét nghiệm có trình độ đại học hoặc sau đại học về chuyên ngành Vi
2. Phương tiện, hóa chất
Phương tiện, hóa chất như ví dụ dưới đây hoặc tương đương.
Trang thiết bị
- Que tăm bông lấy bệnh phẩm.
- Ống nghiệm (được cung cấp sẵn trong bộ kit).
- Nước muối sinh lý.
- Đồng hồ bấm giây.
Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
Thực hiện xét nghiệm 02 mẫu/lần
| STT | Chi phí hóa chất, vật tư tiêu hao | Đơn vị | Số lượng |
| 1 | Tăm bông vô trùng | Cái | 1,000 |
| 2 | Lọ vô trùng | Cái | 1,000 |
| 3 | Khay đựng bệnh phẩm | Cái | 0,0001 |
| 4 | Hộp vận chuyển bệnh phẩm | Cái | 0,001 |
| 5 | Sinh phẩm chẩn đoán | Test | 1,000 |
| 6 | Khấu hao sinh phẩm cho chạy chứng, kiểm tra chất lượng | Test | 0,100 |
| 7 | Giấy thấm | Cuộn | 0,100 |
| 8 | Giấy xét nghiệm | Tờ | 2,000 |
| 9 | Sổ lưu kết quả xét nghiệm | Tờ | 0,001 |
| 10 | Bút viết kính | Cái | 0,020 |
| 11 | Bút bi | Cái | 0,010 |
| 12 | Mũ | Cái | 0,020 |
| 13 | Khẩu trang | Cái | 0,020 |
| 14 | Găng tay | Đôi | 0,100 |
| 15 | Găng tay xử lý dụng cụ | Đôi | 0,020 |
| 16 | Quần áo bảo hộ | Bộ | 0,005 |
| 17 | Dung dịch nước rửa tay | ml | 8,000 |
| 18 | Cồn sát trùng tay nhanh | ml | 1,000 |
| 19 | Dung dịch khử trùng | ml | 10,000 |
| 20 | Khăn lau tay | Cái | 0,010 |
3. Bệnh phẩm
Phân của người bệnh
4. Phiếu xét nghiệm
Điền đầy đủ thông tin theo mẫu phiếu yêu cầu
III. CÁC BƯỚC TIẾN HÀNH
Các bước tiến hành thực hiện theo phương tiện, hóa chất được ví dụ ở trên.
1. Lấy bệnh phẩm
- Theo đúng quy định của chuyên ngành Vi sinh: xem chi tiết phụ lục
- Từ chối những bệnh phẩm không đạt yêu cầu: xem chi tiết phụ lục
2. Tiến hành kỹ thuật
Bộ sinh phẩm chẩn đoán SD Bioline Rotavirus (VD).
| Các bước | Xét nghiệm phát hiện Rota virus |
| 1. | – Đưa test cần làm để ổn định ở nhiệt độ phòng trước khi làm. Lấy thanh xét nghiệm cần thiết. |
| 2. | – Hút hút dung dịch pha loãng bệnh phẩm theo hướng dẫn |
| 3. | – Lấy khoảng 50 mg phân bằng que tăm bông vô trùng nhúng vào ống nghiệm có chứa dung dịch pha loãng. |
| 4. | – Xoay tròn que tăm bông để bệnh phẩm hoà vào dung dịch pha loãng theo hướng dẫn. Đậy nắp ống nghiệm đã có bệnh phẩm lại. |
| 5. | – Nhỏ dung dich bệnh phẩm đã pha loãng vào giếng nhỏ bệnh phẩm (có chữ S). |
| 6. | – Đọc kết quả sau 10-20 phút. Quá 20 phút, kết quả không có giá trị. |
IV. NHẬN ĐỊNH KẾT QUẢ
- Âm tính: Chỉ 1 một đường màu xuất hiện ở vùng chứng
- Dương tinh: 2 đường màu xuất hiện ở vùng chứng (C) và vùng thử nghiệm (T).
- Không có giá trị: Không thấy xuất hiện đường màu nào hoặc chỉ có một đường màu tại vùng thử nghiệm (T). Khi đó phải tiến hành làm lại xét nghiệm với một thanh thử khác.
V. NHỮNG SAI SÓT VÀ XỬ TRÍ
- Âm tính giả: Lượng virus đào thải ra ngoài quá thấp, hoặc do sai sót trong quá trình lấy và xử lý mẫu.
- Tham khảo thêm hướng dẫn của nhà sản xuất.
Hồng cầu, bạch cầu trong phân soi tươi
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đích
Phát hiện hồng cầu, bạch cầu trong phân.
2. Nguyên lý
Nhận định hồng cầu, bạch cầu trong phân khi làm tiêu bản soi tươi dưới kính hiển vi quang học dựa trên hình thể, kích thước, và cấu tạo.
II. CHUẨN BỊ
1.Người thực hiện
- Người thực hiện Cán bộ xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành Vi sinh – Ký sinh trùng
- Người nhận định và phê duyệt kết quả: cán bộ có trình độ đại học hoặc sau đại học về chuyên ngành Vi sinh – Ký sinh trùng
2.Phương tiện, hóa chất
Phương tiện, hóa chất như ví dụ dưới đây hoặc tương đương.
Trang thiết bị
- Kính hiển vi quang học
- Tủ an toàn sinh học cấp 2
Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
| STT | Chi phí hóa chất, vật tư tiêu hao | Đơn vị | Số lượng |
| 1 | Lọ lấy bệnh phẩm | Lọ | 1,000 |
| 2 | Que cấy | Cái | 2,000 |
| 3 | Lam kính | Cái | 1,000 |
| 4 | Lá kính | Cái | 2,000 |
| 5 | Bông | Kg | 0,001 |
| 6 | Cồn 90 độ (vệ sinh dụng cụ) | ml | 10,000 |
| 7 | Panh | Cái | 0,0001 |
| 8 | Khay đựng bệnh phẩm | Cái | 0,0001 |
| 9 | Hộp vận chuyển bệnh phẩm | Cái | 0,0001 |
| 10 | Nước muối sinh lý | ml | 5,000 |
| 11 | Lugol | ml | 2,000 |
| 13 | Pipet nhựa | Cái | 2,000 |
| 14 | Axit ngâm lam | ml | 10,000 |
| 15 | Mũ | Cái | 0,020 |
| 16 | Khẩu trang | Cái | 0,020 |
| 17 | Găng tay | Đôi | 3,000 |
| 18 | Găng tay xử lý dụng cụ | Đôi | 0,020 |
| 19 | Quần áo bảo hộ | Bộ | 0,001 |
| 20 | Bút viết kính | Cái | 0,020 |
| 21 | Bút bi | Cái | 0,010 |
| 22 | Bật lửa | Cái | 0,010 |
| 23 | Sổ lưu kết quả xét nghiệm | Quyển | 0,001 |
| 24 | Cồn sát trùng tay nhanh | ml | 1,000 |
| 25 | Dung dịch nước rửa tay | ml | 8,000 |
| 26 | Khăn lau tay | Cái | 0,010 |
| 27 | Giấy trả kết quả xét nghiệm | Tờ | 2,000 |
| 28 | QC (nếu thực hiện) * | 0,1 | |
| 29 | EQAS (nếu thực hiện) * | 0,005 |
* Ghi chú:
- Chi phí nội kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình nội kiểm (QC) là 1/10 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lượng
≥ 10 mẫu cho 1 lần tiến hành kỹ thuật).
- Chi phí ngoại kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình ngoại kiểm (EQAS) là 1/200 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lần ngoại kiểm trung bình 2 lần/1 năm).
3. Bệnh phẩm: Phân
4. Phiếu xét nghiệm
Điền đầy đủ thông tin theo mẫu phiếu yêu cầu
III. CÁC BƯỚC TIẾN HÀNH
Các bước tiến hành thực hiện theo phương tiện, hóa chất được ví dụ ở trên.
1. Lấy bệnh phẩm
Theo đúng quy định của chuyên ngành Vi sinh ( xem Phụ lục 4).
2. Tiến hành kỹ thuật
- Nhỏ dung dịch NaCL 9 ‰ và dung dịch Lugol 1% lên trên một lam kính.
- Dùng que lấy một lượng phân (bao kín đầu que) hòa đều với giọt NaCL 9‰ đến khi có màu đục, làm tương tự đối với giọt Lugol 1%.
- Đặt lá kính lên trên giọt dung dịch.
- Quan sát kính hiển vi ở vật kính
IV. NHẬN ĐỊNH KẾT QUẢ
1. Dương tính
- Hồng cầu: hình tròn kích thước 7-8µm màu hồng nhạt, trung tâm nhạt màu.
- Hồng cầu thoái hóa: bờ răng cưa không đều.
- Bạch cầu đa nhân hình tròn kích thước lớn 10 – 15µm.
- Bạch cầu đơn nhân hình tròn, bầu dục, đa giác kích thước 20 – 25 µm.
2. Âm tính
Không tìm thấy hồng cầu, bạch cầu.
V. NHỮNG SAI SÓT VÀ XỬ TRÍ
1. Sai sót
- Nhỏ quá nhiều dung dịch lên lam kính.
- Làm tiêu bản quá dầy hoặc quá mỏng.
2. Xử trí
Đặt tiêu bản trên tờ báo vẫn đọc được chữ là đạt. Nếu làm tiêu bản quá dầy sẽ khó soi, làm mỏng quá sẽ bỏ sót không phát hiện được hồng cầu, bạch cầu.
Hồng cầu trong phân test nhanh
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đích
Phát hiện hồng cầu trong phân.
2. Nguyên lý
Phát hiện hemoglobin trong phân dựa trên nguyên lý sắc ký miễn dịch.
II. CHUẨN BỊ
1. Người thực hiện
- Người thực hiện: Cán bộ xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành Vi sinh – Ký sinh trùng.
- Người nhận định và phê duyệt kết quả: Cán bộ có trình độ đại học hoặc sau đại học về chuyên ngành Vi sinh – Ký sinh trùng
2. Phương tiện, hóa chất
Phương tiện, hóa chất như ví dụ dưới đây hoặc tương đương.
Trang thiết bị
- Đồng hồ bấm giờ (nếu có)
- Tủ an toàn sinh học cấp 2
Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
| STT | Chi phí hóa chất, vật tư tiêu hao | Đơn vị | Số lượng |
| 1 | Lọ lấy bệnh phẩm | Lọ | 1,000 |
| 2 | Que cấy | Cái | 2,000 |
| 3 | Bông | Kg | 0,001 |
| 4 | Cồn 90 độ (vệ sinh dụng cụ) | ml | 10,000 |
| 5 | Panh | Cái | 0,0001 |
| 6 | Khay đựng bệnh phẩm | Cái | 0,0001 |
| 7 | Hộp vận chuyển bệnh phẩm | Cái | 0,0001 |
| 9 | Sinh phẩm chẩn đoán | Test | 1,000 |
| 10 | Pipet nhựa | Cái | 2,000 |
| 11 | Ống nghiệm thủy tinh | Ống | 1,000 |
| 12 | Mũ | Cái | 0,020 |
| 13 | Khẩu trang | Cái | 0,020 |
| 14 | Găng tay | Đôi | 3,000 |
| 15 | Găng tay xử lý dụng cụ | Đôi | 0,020 |
| 16 | Quần áo bảo hộ | Bộ | 0,001 |
| 17 | Bút viết kính | Cái | 0,020 |
| 18 | Bút bi | Cái | 0,010 |
| 19 | Bật lửa | Cái | 0,010 |
| 20 | Sổ lưu kết quả xét nghiệm | Quyển | 0,001 |
| 21 | Cồn sát trùng tay nhanh | ml | 1,000 |
| 22 | Dung dịch nước rửa tay | ml | 8,000 |
| 23 | Khăn lau tay | Cái | 0,010 |
| 24 | Giấy trả kết quả xét nghiệm | Tờ | 2,000 |
| 25 | QC (nếu thực hiện) * | 0,1 | |
| 26 | EQAS (nếu thực hiện) * | 0,005 |
* Ghi chú:
- Chi phí nội kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình nội kiểm (QC) là 1/10 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lượng
≥ 10 mẫu cho 1 lần tiến hành kỹ thuật).
- Chi phí ngoại kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình ngoại kiểm (EQAS) là 1/200 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lần ngoại kiểm trung bình 2 lần/1 năm).
3.Bệnh phẩm
Phân
4.Phiếu xét nghiệm
Điền đầy đủ thông tin theo mẫu phiếu yêu cầu
III. CÁC BƯỚC TIẾN HÀNH
Các bước tiến hành thực hiện theo phương tiện, hóa chất được ví dụ ở trên.
1. Lấy bệnh phẩm
Theo đúng quy định của chuyên ngành Vi sinh ( xem Phụ lục 4).
2.Tiến hành kỹ thuật
Bộ sinh phẩm chẩn đoán Hemosure iFOB Test.
- Lấy thanh thử ra khỏi bao để ở nhiệt độ phòng .
- Dùng que lấy bệnh phẩm (bao kín đầu que) nhúng que vào lọ dung dịch trong test thử, lắc đều.
- Nhỏ 3 giọt dung dịch trên vào thanh thử.
- Đọc kết quả trong vòng 5- 10 phút.
IV. NHẬN ĐỊNH KẾT QUẢ
1. Dương tính
Xuất hiện 2 vạch trên thanh thử ở vị trí C và T.
2. Âm tính
Xuất hiện 1 vạch trên thanh thử ở vị trí C.
3. Không có giá trị
Không thấy xuất hiện vạch nào trên thanh thử. Phải tiến hành làm lại xét nghiệm với một thanh thử khác.
V. NHỮNG SAI SÓT VÀ XỬ TRÍ
Đọc kết quả sau quá 10 phút dễ gây phản ứng dương tính giả. Nên có đồng hồ đặt giờ để đọc kết quả đúng giờ qui định.
Đơn bào đường ruột soi tươi
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đích
Phát hiện đơn bào đường ruột gây bệnh (Entamoeba histolytica, Giardia lamblia, Isospora belli, Trichomonas intestinalis…) trong phân.
2. Nguyên lý
Đơn bào đường ruột gây bệnh được phát hiện qua hình thể, kích thước, tính chất di động và bắt màu trong môi trường có NaCL 9‰ và Lugol 1% soi dưới kính hiển vi quang học.
II. CHUẨN BỊ
1. Người thực hiện
- Người thực hiện: Cán bộ xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành Vi sinh – Ký sinh trùng.
- Người nhận định và phê duyệt kết quả: Cán bộ có trình độ đại học hoặc sau đại học về chuyên ngành Vi sinh – Ký sinh trùng
2. Phương tiện, hóa chất
Phương tiện, hóa chất như ví dụ dưới đây hoặc tương đương.
Trang thiết bị
- Kính hiển vi quang học
- Tủ an toàn sinh học cấp 2
Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
| STT | Chi phí hóa chất, vật tư tiêu hao | ĐƠN VỊ | SỐ LƯỢNG |
| 1 | Lọ lấy bệnh phẩm | Lọ | 1,000 |
| 2 | Que cấy | Cái | 2,000 |
| 3 | Lam kính | Cái | 2,000 |
| 4 | Lá kính | Cái | 2,000 |
| 5 | Bông | Kg | 0,001 |
| 6 | Cồn 900 (vệ sinh dụng cụ) | ml | 10,000 |
| 7 | Panh | Cái | 0,0001 |
| 8 | Khay đựng bệnh phẩm | Cái | 0,0001 |
| 9 | Hộp vận chuyển bệnh phẩm | Cái | 0,0001 |
| 10 | Nước muối sinh lý | ml | 5,000 |
| 11 | Lugol | ml | 2,000 |
| 12 | Pipet nhựa | Cái | 2,000 |
| 13 | Axit ngâm lam | ml | 10,000 |
| 14 | Mũ | Cái | 0,020 |
| 15 | Khẩu trang | Cái | 0,020 |
| 16 | Găng tay | Đôi | 3,000 |
| 17 | Găng tay xử lý dụng cụ | Đôi | 0,020 |
| 18 | Quần áo bảo hộ | Bộ | 0,001 |
| 19 | Bút viết kính | Cái | 0,020 |
| 20 | Bút bi | Cái | 0,010 |
| 21 | Bật lửa | Cái | 0,010 |
| 22 | Sổ lưu kết quả xét nghiệm | Quyển | 0,001 |
| 23 | Cồn sát trùng tay nhanh | ml | 1,000 |
| 24 | Dung dịch nước rửa tay | ml | 8,000 |
| 25 | Khăn lau tay | Cái | 0,010 |
| 26 | Giấy trả kết quả xét nghiệm | Tờ | 2,000 |
| 27 | QC (nếu thực hiện) * | 0,1 | |
| 28 | EQAS (nếu thực hiện) * | 0,005 |
* Ghi chú:
- Chi phí nội kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình nội kiểm (QC) là 1/10 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lượng ≥ 10 mẫu cho 1 lần tiến hành kỹ thuật).
- Chi phí ngoại kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình ngoại kiểm (EQAS) là 1/200 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lần ngoại kiểm trung bình 2 lần/1 năm).
3. Bệnh phẩm
Phân
4. Phiếu xét nghiệm
Điền đầy đủ thông tin theo mẫu phiếu yêu cầu
III. CÁC BƯỚC TIẾN HÀNH
Các bước tiến hành thực hiện theo phương tiện, hóa chất được ví dụ ở trên.
1. Lấy bệnh phẩm
Theo đúng quy định của chuyên ngành Vi sinh ( xem Phụ lục 4).
Lưu ý: – Không lấy phân làm XN khi uống thuốc Bismuth hoặc Barium.
– Mẫu phân làm xét nghiệm tránh lẫn nước tiểu.
2. Tiến hành kỹ thuật
- Nhỏ giọt dung dịch NaCL 9 ‰ và giọt dung dịch Lugol 1% lên trên một lam kính.
- Dùng que lấy một lượng phân (bao kín đầu que) hòa đều vào dung dịch NaCL 9 ‰ đến khi có màu đục, làm tương tự đối với dung dịch
- Đặt lá kính lên trên dung dịch.
- Quan sát kính hiển vi ở vật kính
IV. NHẬN ĐỊNH KẾT QUẢ
1. Dương tính
Quan sát ở vật kính 40X tìm thể hoạt động và bào nang của đơn bào. Thể hoạt động của Amip kích thước 13-30µm chuyển động bằng chân giả.
- Thể hoạt động của Giardia hình thìa kích thước 9-21 x 5-15µm chuyển động bằng
- Trichomonas hình quả lê kích thước 5-12 x 5-6µm chuyển động được nhờ các
- Bào nang Amip hình tròn có vỏ dày bắt màu vàng, kích thước trung bình 12µm bên trong có từ 2-4 nhân.
- Bào nang Giardia hình bầu dục kích thước 10-14 x7-9µm, bên trong có từ 2-4 nhân có thể thấy vết roi cuộn lại trong bào
2. Âm tính
Không thấy thể hoạt động, bào nang của đơn bào đường ruột.
Lưu ý
Trong trường hợp xét nghiệm lần đầu âm tính, để phát hiện KST gây bệnh có thể xét nghiệm 2 mẫu phân tiếp theo trong vòng từ 7-10 ngày.
V. NHỮNG SAI SÓT VÀ XỬ TRÍ
1. Sai sót
- Nhỏ quá nhiều dung dịch lên lam kính .
- Tiêu bản quá dầy hoặc quá mỏng.
2. Xử trí
Đặt tiêu bản trên tờ báo vẫn đọc được chữ là đạt. Nếu làm tiêu bản quá dầy sẽ khó soi, làm mỏng sẽ bỏ sót không phát hiện được đơn bào đường ruột.
Đơn bào đường ruột nhuộm soi
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đích
Phát hiện đơn bào đường ruột gây bệnh (Isospora belli, Cryptosporidium, Cyclospora) trong phân.
2. Nguyên lý
Một số đơn bào đường ruột có đặc điểm kháng cồn/acid nên có thể được phát hiện bằng kỹ thuật nhuộm Ziehl-Neelsen.
II. CHUẨN BỊ
1. Người thực hiện
- Người thực hiện Cán bộ xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành Vi sinh – Ký sinh trùng.
- Người nhận định và phê duyệt kết quả: Cán bộ có trình độ đại học hoặc sau đại học về chuyên ngành Vi sinh – Ký sinh trùng
2. Phương tiện, hóa chất
Phương tiện, hóa chất như ví dụ dưới đây hoặc tương đương.
Trang thiết bị
- Kính hiển vi quang học.
- Tủ an toàn sinh học cấp 2
- Đồng hồ bấm giờ.
Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
| STT | Chi phí hóa chất, vật tư tiêu hao | Đơn vị | Số lượng |
| 1 | Lọ lấy bệnh phẩm | Lọ | 1,000 |
| 2 | Lam kính | Cái | 2,000 |
| 3 | Dầu soi kính | ml | 1,000 |
| 4 | Xylen lau kính | ml | 1,000 |
| 5 | Thuốc nhuộm đỏ Fucsin | ml | 5,000 |
| 6 | Axit H2SO4 | ml | 10,000 |
| 7 | Que cấy | Cái | 1,000 |
| 8 | Cồn tẩy 96 độ | ml | 10,000 |
| 9 | Thuốc nhuộm Xanh methylen | ml | 5,000 |
| 10 | Bông | Kg | 0,001 |
| 11 | Cồn 90 độ (vệ sinh dụng cụ) | ml | 10,000 |
| 12 | Đèn cồn | Cái | 0,0001 |
| 13 | Panh | Cái | 0,0001 |
| 14 | Khay đựng bệnh phẩm | Cái | 0,0001 |
| 15 | Hộp vận chuyển bệnh phẩm | Cái | 0,0001 |
| 16 | Mũ | Cái | 0,020 |
| 17 | Khẩu trang | Cái | 0,020 |
| 18 | Găng tay | Đôi | 3,000 |
| 19 | Găng tay xử lý dụng cụ | Đôi | 0,020 |
| 20 | Quần áo bảo hộ | Bộ | 0,001 |
| 21 | Axit ngâm lam | ml | 10,000 |
| 22 | Ống nghiệm thủy tinh | Ống | 1,000 |
| 23 | Bút viết kính | Cái | 0,020 |
| 24 | Bút bi | Cái | 0,010 |
| 25 | Bật lửa | Cái | 0,010 |
| 26 | Sổ lưu kết quả xét nghiệm | Tờ | 0,001 |
| 27 | Cồn sát trùng tay nhanh | ml | 1,000 |
| 28 | Dung dịch nước rửa tay | ml | 8,000 |
| 29 | Khăn lau tay | Cái | 0,030 |
| 30 | Giấy trả kết quả xét nghiệm | Tờ | 2,000 |
| 31 | QC (nếu thực hiện) * | 0,1 | |
| 32 | EQAS (nếu thực hiện) * | 0,005 |
* Ghi chú:
- Chi phí nội kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình nội kiểm (QC) là 1/10 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lượng ≥ 10 mẫu cho 1 lần tiến hành kỹ thuật).
- Chi phí ngoại kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình ngoại kiểm (EQAS) là 1/200 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lần ngoại kiểm trung bình 2 lần/1 năm).
3. Bệnh phẩm
Phân
4. Phiếu xét nghiệm
Điền đầy đủ thông tin theo mẫu phiếu yêu cầu
III. CÁC BƯỚC TIẾN HÀNH
1. Lấy bệnh phẩm
Theo đúng quy định của chuyên ngành Vi sinh ( xem Phụ lục 4).
2. Tiến hành kỹ thuật
- Dùng que gỗ lấy phân phết lên lam kính, để khô.
- Nhỏ dung dịch đỏ Fucsin phủ kín lên trên bệnh phẩm.
- Rửa nước.
- Tẩy màu bằng H2SO4 5% đến khi hết màu đỏ.
- Rửa nước
- Nhỏ dung dịch xanh
- Rửa nước.
- Quan sát dưới kính hiển vi vật kính 10X-
IV. NHẬN ĐỊNH KẾT QUẢ
1. Dương tính
- Nang trứng của Cryptosporidium hình tròn bắt màu đỏ kích thước từ 4- 6µm.
- Nang trứng của Cyclospora hình tròn bắt màu đỏ kích thước từ 8- 10µm.
- Nang trứng của Isospora hình bầu dục bắt màu đỏ kích thước 20- 30 X 10- 19µm.
2. Âm tính
Không tìm thấy đơn bào đường ruột.
Lưu ý: Trong trường hợp xét nghiệm lần đầu âm tính, để phát hiện KST gây bệnh có thể xét nghiệm 2 mẫu phân tiếp theo trong vòng từ 7-10 ngày.
V. NHỮNG SAI SÓT VÀ XỬ TRÍ
1. Sai sót
Tẩy chưa hết màu đỏ Fucsin.
2. Xử trí
Nếu bệnh phẩm dày để đủ thời gian nhưng vẫn còn màu đỏ Fucsin cần phải tẩy lại lần 2 bằng H2SO4 5% đến khi bệnh phẩm phai hết màu đỏ.
Trứng giun, sán soi tươi
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đích
Phát hiện trứng giun, sán trong phân.
2. Nguyên lý
Nhận định trứng giun, sán dựa vào hình thể, kích thước, cấu tạo và tính chất bắt màu khi soi tươi.
II. CHUẨN BỊ
1. Người thực hiện
- Người thực hiện Cán bộ xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành Vi sinh – Ký sinh trùng.
- Người nhận định và phê duyệt kết quả: Cán bộ có trình độ đại học hoặc sau đại học về chuyên ngành Vi sinh – Ký sinh trùng
3. Phương tiện, hóa chất
Phương tiện, hóa chất như ví dụ dưới đây hoặc tương đương.
Trang thiết bị
Kính hiển vi quang học Tủ an toàn sinh học cấp 2
Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
| STT | Chi phí hóa chất, vật tư tiêu hao | Đơn vị | Số lượng |
| 1 | Lọ lấy bệnh phẩm | Lọ | 1,000 |
| 2 | Que cấy | Cái | 2,000 |
| 3 | Lam kính | Cái | 2,000 |
| 4 | Lá kính | Cái | 2,000 |
| 5 | Bông | Kg | 0,001 |
| 6 | Cồn 900 (vệ sinh dụng cụ) | ml | 10,000 |
| 7 | Panh | Cái | 0,0001 |
| 8 | Khay đựng bệnh phẩm | Cái | 0,0001 |
| 9 | Hộp vận chuyển bệnh phẩm | Cái | 0,0001 |
| 10 | Nước muối sinh lý | ml | 5,000 |
| 11 | Lugol | ml | 2,000 |
| 13 | Pipet nhựa | Cái | 2,000 |
| 14 | Axit ngâm lam | ml | 10,000 |
| 15 | Mũ | Cái | 0,020 |
| 16 | Khẩu trang | Cái | 0,020 |
| 17 | Găng tay | Đôi | 3,000 |
| 18 | Găng tay xử lý dụng cụ | Đôi | 0,020 |
| 19 | Quần áo bảo hộ | Bộ | 0,001 |
| 20 | Bút viết kính | Cái | 0,020 |
| 21 | Bút bi | Cái | 0,010 |
| 22 | Bật lửa | Cái | 0,010 |
| 23 | Sổ lưu kết quả xét nghiệm | Quyển | 0,001 |
| 24 | Cồn sát trùng tay nhanh | ml | 1,000 |
| 25 | Dung dịch nước rửa tay | ml | 8,000 |
| 26 | Khăn lau tay | Cái | 0,010 |
| 27 | Giấy trả kết quả xét nghiệm | Tờ | 2,000 |
| 28 | QC (nếu thực hiện) * | 0,1 | |
| 29 | EQAS (nếu thực hiện) * | 0,005 |
* Ghi chú:
- Chi phí nội kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình nội kiểm (QC) là 1/10 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lượng ≥ 10 mẫu cho 1 lần tiến hành kỹ thuật).
- Chi phí ngoại kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình ngoại kiểm (EQAS) là 1/200 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lần ngoại kiểm trung bình 2 lần/1 năm).
3. Bệnh phẩm
Phân
4. Phiếu xét nghiệm
Điền đầy đủ thông tin theo mẫu phiếu yêu cầu
III. CÁC BƯỚC TIẾN HÀNH
1.Lấy bệnh phẩm
Theo đúng quy định của chuyên ngành Vi sinh ( xem Phụ lục 4).
2. Tiến hành kỹ thuật
- Nhỏ dung dịch NaCL 9 ‰ và dung dịch Lugol 1% lên trên 1 lam kính.
- Dùng que lấy một lượng phân (bao kín đầu que) hòa đều vào giọt dung dịch NaCL 9 ‰ đến khi có màu đục, làm tương tự đối với giọt dung dịch Lugol 1%.
- Đặt lá kính lên trên giọt dung dịch.
- Quan sát kính hiển vi ở vật kính 10X-
IV. NHẬN ĐỊNH KẾT QUẢ
1. Dương tính
- Trứng giun đũa hình tròn hoặc bầu dục kích thước 35-50 x 45-75mm, ngoài cùng là lớp albumin xù xì bắt màu vàng, vỏ dầy, trong là khối nhân sẫm màu. Ngoài ra có thể còn gặp trứng giun đũa mất tầng
- Trứng giun đũa không thụ tinh hình bầu dục kích thước 43- 47 x 85- 95µm. Vỏ mỏng ít xù xì bên trong có những tế bào hoàng thể.
- Trứng giun móc hình bầu dục kích thước 40-60mm màu trong vỏ mỏng, trong là khối nhân phân chia từ 2-4 phần .
- Trứng giun tóc hình bầu dục, kích thước 22-50mm giống hình quả cau, màu vàng vỏ dầy, 2 cực có 2 nắp.
- Trứng sán lá gan nhỏ bắt màu vàng hình bầu dục một đầu có nắp một đầu có gai, kích thước 27-35 x 12-19µm.
- Trứng sán lá gan lớn hình bầu dục kích thước lớn từ 130-150 X 63-90µm, màu vàng nhạt vỏ mỏng, một đầu có nắp.
- Trứng sán lá phổi hình bầu dục màu vàng nâu sẫm kích thước lớn từ 80- 120 X 50- 70µm, ở đầu có nắp trong trứng thấy có 1 đám tế bào.
- Trứng sán dây hình tròn vỏ dầy màu nâu sẫm kích thước từ 36-51µm.
2. Âm tính
Không thấy trứng giun, sán.
Lưu ý
Trong trường hợp xét nghiệm lần đầu âm tính, để phát hiện KST gây bệnh có thể xét nghiệm 2 mẫu phân tiếp theo trong vòng từ 7-10 ngày.
V. NHỮNG SAI SÓT VÀ XỬ TRÍ
1. Sai sót
- Nhỏ quá nhiều dung dịch lên lam kính .
- Làm tiêu bản quá dầy hoặc quá mỏng.
2. Xử trí
Đặt tiêu bản trên tờ báo vẫn đọc được chữ là đạt. Nếu làm tiêu bản quá dầy sẽ khó soi, làm mỏng quá sẽ bỏ sót trứng giun sán.
Trứng giun soi tập trung
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đích
Phát hiện trứng giun đũa, tóc, móc trong phân.
2. Nguyên lý
Nước muối bão hòa có tỷ trọng lớn hơn tỷ trọng của trứng giun đũa, tóc, móc vì vậy sẽ làm cho trứng giun nổi lên trên bề mặt của dung dịch và bám vào bề mặt của lá kính.
II. CHUẨN BỊ
1.Người thực hiện
- Người thực hiện: Cán bộ xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành Vi sinh – Ký sinh trùng.
- Người nhận định và phê duyệt kết quả: Cán bộ có trình độ đại học hoặc sau đại học về chuyên ngành Vi sinh – Ký sinh trùng
2. Phương tiện, hóa chất
Phương tiện, hóa chất như ví dụ dưới đây hoặc tương đương.
Trang thiết bị
- Kính hiển vi
- Tủ an toàn sinh học cấp 2
- Đồng hồ bấm giờ
Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
| STT | Chi phí hóa chất, vật tư tiêu hao | Đơn vị | Số lượng |
| 1 | Lọ lấy bệnh phẩm | Lọ | 1,000 |
| 2 | Que cấy | Cái | 2,000 |
| 3 | Lam kính | Cái | 1,000 |
| 4 | Lá kính | Cái | 1,000 |
| 5 | Bông | Kg | 0,001 |
| 6 | Cồn 90 độ (vệ sinh dụng cụ) | ml | 10,000 |
| 7 | Panh | Cái | 0,0001 |
| 8 | Khay đựng bệnh phẩm | Cái | 0,0001 |
| 9 | Hộp vận chuyển bệnh phẩm | Cái | 0,0001 |
| 10 | Nước muối bão hòa | ml | 15,000 |
| 11 | Sinh phẩm chẩn đoán | Test | 1,000 |
| 12 | Pipet nhựa | Cái | 2,000 |
| 13 | Axit ngâm lam | ml | 10,000 |
| 14 | Mũ | Cái | 0,020 |
| 15 | Khẩu trang | Cái | 0,020 |
| 16 | Găng tay | Đôi | 3,000 |
| 17 | Găng tay xử lý dụng cụ | Đôi | 0,020 |
| 18 | Quần áo bảo hộ | Bộ | 0,001 |
| 19 | Bút viết kính | Cái | 0,020 |
| 20 | Bút bi | Cái | 0,010 |
| 21 | Bật lửa | Cái | 0,010 |
| 22 | Sổ lưu kết quả xét nghiệm | Quyển | 0,001 |
| 23 | Cồn sát trùng tay nhanh | ml | 1,000 |
| 24 | Dung dịch nước rửa tay | ml | 8,000 |
| 25 | Khăn lau tay | Cái | 0,010 |
| 26 | Giấy trả kết quả xét nghiệm | Tờ | 2,000 |
| 27 | QC (nếu thực hiện) * | 0,1 | |
| 28 | EQAS (nếu thực hiện) * | 0,005 |
* Ghi chú:
- Chi phí nội kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình nội kiểm (QC) là 1/10 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lượng ≥ 10 mẫu cho 1 lần tiến hành kỹ thuật).
- Chi phí ngoại kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình ngoại kiểm (EQAS) là 1/200 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lần ngoại kiểm trung bình 2 lần/1 năm).
3. Bệnh phẩm
Phân
4. Phiếu xét nghiệm
Điền đầy đủ thông tin theo mẫu phiếu yêu cầu
III. CÁC BƯỚC TIẾN HÀNH
1. Lấy bệnh phẩm
Theo đúng quy định của chuyên ngành Vi sinh ( xem Phụ lục 4).
2. Tiến hành kỹ thuật
- Cho nước muối bão hòa vào lọ đựng bệnh phẩm (1/3 lọ), dùng que đánh tan bệnh phẩm.
- Nhỏ nước muối bão hòa vào gần đầy lọ gạt bỏ bệnh phẩm nổi trên bề mặt sau đó nhỏ tiếp dung dịch vào đầy miệng lọ.
- Đậy lá kính lên trên lọ bệnh phẩm để thời gian 15 phút.
- Nhấc lá kính đặt trên lam kính.
- Quan sát kính hiển vi ở vật kính
IV. NHẬN ĐỊNH KẾT QUẢ
1. Dương tính
Quan sát tất cả các vi trường ở vật kính 10X tìm trứng giun, chọn vi trường có số trứng giun cao nhất để đánh giá kết quả:
- Trứng giun đũa hình tròn hoặc bầu dục kích thước 35-50 x 45-75mm, ngoài cùng là lớp Albumin xù xì bắt màu vàng, vỏ dầy, trong là khối nhân sẫm màu. Ngoài ra có thể còn gặp trứng giun đũa mất tầng
- Trứng giun móc hình bầu dục kích thước 40-60mm màu trong vỏ mỏng, trong là khối nhân phân chia từ 2-4 .
- Trứng giun tóc hình bầu dục, kích thước 22-50mm giống hình quả cau, màu vàng vỏ dầy, 2 cực có 2 nắp.
Ghi tên trứng giun và mức độ nhiễm:
- 1 trứng giun / vi trường : (+)
- 2 – 5 trứng giun / vi trường : (++)
- 6 – 20 trứng giun / vi trường : (+++)
- > 20 trứng giun / vi trường : (++++)
2. Âm tính
Không thấy trứng giun
Lưu ý
Trong trường hợp xét nghiệm lần đầu âm tính, để phát hiện KST gây bệnh có thể xét nghiệm 2 mẫu phân tiếp theo trong vòng từ 7-10 ngày.
V. NHỮNG SAI SÓT VÀ XỬ TRÍ
1. Sai sót
- Không gạt bỏ bệnh phẩm nổi trên miệng lọ, kết quả có thể bị
- Để thời gian quá ngắn trứng giun chưa kịp nổi trên bề mặt dung dịch.
2. Xử trí
- Gạt bỏ sạch bệnh phẩm nổi trên mặt dung dịch.
- Để đủ thời gian quy định.
Strongyloides stercoralis (Giun lươn) ấu trùng soi tươi
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đích
Phát hiện ấu trùng S. stercoralis trong phân.
2. Nguyên lý
Ấu trùng S. stercoralis được phát hiện dựa vào hình thể, kích thước và chuyển động khi soi tươi phân.
II. CHUẨN BỊ
1.Người thực hiện
- Người thực hiện: Cán bộ xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành Vi sinh – Ký sinh trùng.
- Người nhận định và phê duyệt kết quả: Cán bộ có trình độ đại học hoặc sau đại học về chuyên ngành Vi sinh – Ký sinh trùng
2.Phương tiện, hóa chất
Phương tiện, hóa chất như ví dụ dưới đây hoặc tương đương.
Trang thiết bị
- Kính hiển vi quang học
- Tủ an toàn sinh học cấp 2
Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
| STT | Chi phí hóa chất, vật tư tiêu hao | Đơn vị | Số lượng |
| 1 | Lọ lấy bệnh phẩm | Lọ | 1,000 |
| 2 | Que cấy | Cái | 2,000 |
| 3 | Lam kính | Cái | 1,000 |
| 4 | Lá kính | Cái | 1,000 |
| 5 | Bông | Kg | 0,001 |
| 6 | Cồn 900 (vệ sinh dụng cụ) | ml | 10,000 |
| 7 | Panh | Cái | 0,0001 |
| 8 | Khay đựng bệnh phẩm | Cái | 0,0001 |
| 9 | Hộp vận chuyển bệnh phẩm | Cái | 0,0001 |
| 10 | Nước muối sinh lý | ml | 5,000 |
| 11 | Pipet nhựa | Cái | 2,000 |
| 12 | Axit ngâm lam | ml | 10,000 |
| 13 | Mũ | Cái | 0,020 |
| 14 | Khẩu trang | Cái | 0,020 |
| 15 | Găng tay | Đôi | 3,000 |
| 16 | Găng tay xử lý dụng cụ | Đôi | 0,020 |
| 17 | Quần áo bảo hộ | Bộ | 0,001 |
| 18 | Bút viết kính | Cái | 0,020 |
| 19 | Bút bi | Cái | 0,010 |
| 20 | Bật lửa | Cái | 0,010 |
| 21 | Sổ lưu kết quả xét nghiệm | Quyển | 0,001 |
| 22 | Cồn sát trùng tay nhanh | ml | 1,000 |
| 23 | Dung dịch nước rửa tay | ml | 8,000 |
| 24 | Khăn lau tay | Cái | 0,010 |
| 25 | Giấy trả kết quả xét nghiệm | Tờ | 2,000 |
| 26 | QC (nếu thực hiện) * | 0,1 | |
| 27 | EQAS (nếu thực hiện) * | 0,005 |
* Ghi chú:
- Chi phí nội kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình nội kiểm (QC) là 1/10 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lượng ≥ 10 mẫu cho 1 lần tiến hành kỹ thuật).
- Chi phí ngoại kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình ngoại kiểm (EQAS) là 1/200 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lần ngoại kiểm trung bình 2 lần/1 năm).
3. Bệnh phẩm
Phân
4. Phiếu xét nghiệm
Điền đầy đủ thông tin theo mẫu phiếu yêu cầu
III. CÁC BƯỚC TIẾN HÀNH
1.Lấy bệnh phẩm
Dùng que sạch lấy phân ở nhiều vị trí, cho vào lọ sạch có dán nhãn ghi đủ các thông tin tên, tuổi người bệnh, khoa phòng gửi xét nghiệm, ngày giờ lấy bệnh phẩm.
Thời gian để mẫu làm xét nghiệm không quá 1 giờ.
2. Tiến hành kỹ thuật
- Nhỏ dung dịch NaCL 9 ‰ lên lam kính.
- Dùng que lấy bệnh phẩm hòa lên trên dung dịch NaCL 9 ‰ đến khi đục.
- Đặt lá kính lên trên giọt dung dịch.
- Quan sát kính hiển vi ở vật kính 10X-
IV. NHẬN ĐỊNH KẾT QUẢ
1. Dương tính
- Ấu trùng giun lươn có kích thước 16 x 220µm, chuyển động.
- Phân biệt ấu trùng giun lươn và ấu trùng giun móc, mỏ: hình thể 2 loại ấu trùng khó có thể phân biệt, nhưng ấu trùng giun lươn xuất hiện ngay sau khi phân mới bài xuất còn ấu trùng giun móc, mỏ xuất hiện muộn (18- 24 giờ).
2. Âm tính
Không thấy ấu trùng giun lươn.
V. NHỮNG SAI SÓT VÀ XỬ TRÍ
1. Sai sót
- Nhỏ quá nhiều dung dịch lên lam kính.
- Làm tiêu bản quá dầy hoặc quá mỏng.
2. Xử trí
Nhỏ dung dịch vừa phải.
Plasmodium (Ký sinh trùng sốt rét) nhuộm soi định tính
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đích
Phát hiện ký sinh trùng sốt rét trong máu.
2. Nguyên lý
Nhận định ký sinh trùng sốt rét trong máu nhuộm Giemsa dựa trên hình thể, cấu tạo, kích thước và tính chất bắt màu.
II. CHUẨN BỊ
1.Người thực hiện
- Người thực hiện Cán bộ xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành Vi sinh – Ký sinh trùng.
- Người nhận định và phê duyệt kết quả: Cán bộ có trình độ đại học hoặc sau đại học về chuyên ngành Vi sinh – Ký sinh trùng
2.Phương tiện, hóa chất
Phương tiện, hóa chất như ví dụ dưới đây hoặc tương đương.
Trang thiết bị
- Kính hiển
- Tủ an toàn sinh học cấp 2
- Đồng hồ bấm giờ
Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
| STT | Chi phí hóa chất, vật tư tiêu hao | Đơn vị | Số lượng |
| 1 | Tube lấy bệnh phẩm | Cái | 1,000 |
| 2 | Que cấy | Cái | 1,000 |
| 4 | Lam kính | Cái | 2,000 |
| 5 | Giemsa cốt | ml | 1,000 |
| 6 | Dung dịch đệm | ml | 10,000 |
| 7 | Bông | Kg | 0,001 |
| 8 | Cồn 96 độ (vệ sinh dụng cụ) | ml | 10,000 |
| 9 | Panh | Cái | 0,0001 |
| 10 | Khay đựng bệnh phẩm | Cái | 0,0001 |
| 11 | Hộp vận chuyển bệnh phẩm | Cái | 0,0001 |
| 12 | Pipet nhựa | Cái | 2,000 |
| 13 | Axit ngâm lam | ml | 10,000 |
| 14 | Mũ | Cái | 0,100 |
| 15 | Khẩu trang | Cái | 0,100 |
| 16 | Găng tay | Đôi | 3,000 |
| 17 | Găng tay xử lý dụng cụ | Đôi | 0,020 |
| 18 | Quần áo bảo hộ | Bộ | 0,001 |
| 19 | Dung dịch rửa tay | ml | 8,000 |
| 20 | Khăn lau tay | Cái | 0,010 |
| 21 | Bút viết kính | Cái | 0,020 |
| 22 | Bút bi | Cái | 0,010 |
| 23 | Bật lửa | Cái | 0,010 |
| 24 | Sổ lưu kết quả xét nghiệm | Quyển | 0,001 |
| 25 | Cồn sát trùng tay nhanh | ml | 1,000 |
| 26 | Đũa thủy tinh | Cái | 1,000 |
| 27 | Giấy trả kết quả xét nghiệm | Tờ | 2,000 |
| 28 | QC (nếu thực hiện) * | 0,1 | |
| 29 | EQAS (nếu thực hiện) * | 0,005 |
Ghi chú:
- Chi phí nội kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình nội kiểm (QC) là 1/10 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lượng ≥ 10 mẫu cho 1 lần tiến hành kỹ thuật).
- Chi phí ngoại kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình ngoại kiểm (EQAS) là 1/200 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lần ngoại kiểm trung bình 2 lần/1 năm).
3. Bệnh phẩm
Máu toàn phần có chống đông.
4. Phiếu xét nghiệm
Điền đầy đủ thông tin theo mẫu phiếu yêu cầu
III. CÁC BƯỚC TIẾN HÀNH
Các bước tiến hành thực hiện theo phương tiện, hóa chất được ví dụ ở trên.
1. Lấy bệnh phẩm
Theo đúng quy định của chuyên ngành Vi sinh ( xem Phụ lục 4).
2. Tiến hành kỹ thuật
- Làm tiêu tiêu bản giọt máu đặc và giọt máu đàn để khô.
- Cố định giọt máu đàn bằng cồn 96°.
- Pha dung dịch Giemsa cốt với dung dịch đệm nồng độ 10%.
- Nhuộm lam với dung dịch Giemsa đã pha để 10 phút.
- Rửa nước, để khô.
- Quan sát kính hiển vi vật kính
IV. NHẬN ĐỊNH KẾT QUẢ
1. Dương tính
- Có 4 loài ký sinh trùng sốt rét gây bệnh cho người
Plasmodium falciparum, Plasmodium vivax, Plasmodium malariae, Plasmodium ovale.
- Các thể gặp khi xét nghiệm máu
- Plasmodium falciparum: Thể tư dưỡng, thể giao bào ở máu ngoại vi, hiếm gặp thể phân liệt.
- Plasmodium vivax, Plasmodium malariae, Plasmodium ovale: Cả 3 thể: thể tư dưỡng, thể phân liệt, thể giao bào ở máu ngoại
Đánh giá mức độ nhiễm KSTSR ở giọt máu đặc theo 4 mức độ
– 1 – 10 KST / 100 vi trường: (+).
– 11 – 100 KST / 100 vi trường: (++).
– 1 – 10 KST / 1 vi trường: (+++).
– > 10 KST / 1 vi trường: (++++).
2. Âm tính
Không tìm thấy ký sinh trùng sốt rét.
V. NHỮNG SAI SÓT VÀ XỬ TRÍ
1. Sai sót
Giọt máu đặc bị bong sau khi nhuộm do lấy máu quá nhiều hoặc khi rửa dưới vòi nước chảy mạnh.
2. Xử trí
Lấy máu vừa phải, rửa dưới vòi nước chảy nhẹ hoặc đưa vào trong chậu rửa.
202. Phthirus pubis (Rận mu) soi tươi
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đích
Phát hiện hình thái Phthirus pubis gây bệnh ngoài da
2. Nguyên lý
Dưới tác dụng của KOH 10% biểu mô sừng mềm và mỏng do đó bộc lộ hình thái Phthirus pubis.
II. CHUẨN BỊ
1. Người thực hiện
- Người thực hiện: Cán bộ xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành Vi sinh – Ký sinh trùng.
- Người nhận định và phê duyệt kết quả: Cán bộ có trình độ đại học hoặc sau đại học về chuyên ngành Vi sinh – Ký sinh trùng
2. Phương tiện, hóa chất
Phương tiện, hóa chất như ví dụ dưới đây hoặc tương đương.
Trang thiết bị
Bàn lấy bệnh phẩm
Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
| STT | Chi phí hóa chất, vật tư tiêu hao | Đơn vị | Số lượng |
| 1 | Lược mau | Cái | 1,000 |
| 2 | Giấy trắng | Tờ | 1,000 |
| 3 | Găng tay | Đôi | 1,000 |
| 4 | Kính núp | Cái | 1,000 |
3. Bệnh phẩm
Vẩy da, sợi lông mu
4. Phiếu xét nghiệm
Điền đầy đủ thông tin theo mẫu phiếu yêu cầu
III. CÁC BƯỚC TIẾN HÀNH
1.Lấy bệnh phẩm
- Dùng kính lúp soi vùng lông và da mu
- Chú ý vùng chân lông tìm rận mu
- Ở thân lông có thể tìm thấy trứng rận
2. Các bước tiến hành
- Dùng lược mau chải từ chân lông ra ngọn một cách nhẹ nhàng .
- Đặt tờ giấy trắng vuông góc vùng da mu và song song với lược
- Dùng kính lúp soi vào tờ giấy trắng tìm rận hoặc có thể soi vào vùng da mu và thân lông tìm ấu trùng, trứng rận.
VI. NHẬN ĐỊNH KẾT QUẢ
- Rận mu:
+ Cơ thể chia làm 3 phần rõ rệt: Đầu có vòi, ăng ten, mắt đơn, ngực có 3 đốt, bụng có 9 đốt.
+ Rận trưởng thành có 3 cặp chân, ấu trùng có 4 cặp chân đối xứng nhau.
- Ngoài ra, có thể thấy trứng của rận bám trên thân lông.
V. NHỮNG SAI XÓT VÀ XỬ TRÍ
1. Sai sót
- Cần phân biệt rận mu với: Chấy, Ghẻ và các loại Rận trên súc vật.
- Người bệnh dùng thuốc diệt ký sinh trùng
2. Xử trí
- Khi tìm thấy rận mu theo đúng mô tả như trên là tiêu chuẩn chẩn đoán xác định.
- Người bệnh bôi thuốc diệt ký sinh trùng phải ngừng từ 3-5 ngày.
Phthirus pubis (Rận mu) nhuộm soi
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đích
Phát hiện hình thái ký sinh trùng Rận gây bệnh ngoài da
2. Nguyên lý
Dưới tác dụng của glycerin hoặc dầu thực vật bộc lộ hình thái Rận
II. CHUẨN BỊ
1. Người thực hiện
- Người thực hiện: Cán bộ xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành Vi sinh – Ký sinh trùng.
- Người nhận định và phê duyệt kết quả: Cán bộ có trình độ đại học hoặc sau đại học về chuyên ngành Vi sinh – Ký sinh trùng
2. Phương tiện, hóa chất
Phương tiện, hóa chất như ví dụ dưới đây hoặc tương đương.
Trang thiết bị
- Kính hiển vi quang học
- Dụng cụ sấy lam (nếu có)
Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
| STT | Chi phí hóa chất, vật tư tiêu hao | Đơn vị | Số lượng |
| 1 | Lá kính | Cái | 1,000 |
| 2 | Lam kính | Cái | 2,000 |
| 3 | Lam kính (kiểm chuẩn) | Cái | 0,200 |
| 4 | Dung dịch KOH 10% | Ml | 1,000 |
| 5 | Dao cùn | Cái | 2,000 |
| 6 | Bông | Kg | 0,001 |
| 7 | Cồn 90 độ (vệ sinh dụng cụ) | Ml | 10,000 |
| 8 | Kính lúp | Ml | 10,000 |
| 10 | Đèn cồn | Cái | 0,0001 |
| 11 | Panh | Cái | 0,0001 |
| 12 | Khay đựng bệnh phẩm | Cái | 0,0001 |
| 13 | Hộp vận chuyển bệnh phẩm | Cái | 0,0001 |
| 14 | Mũ | Cái | 0,020 |
| 15 | Khẩu trang | Cái | 0,020 |
| 16 | Găng tay | Đôi | 3,000 |
| 17 | Găng tay xử lý dụng cụ | Đôi | 0,020 |
| 18 | Quần áo bảo hộ | Bộ | 0,001 |
| 19 | Ống nghiệm thủy tinh | Ống | 1,000 |
| 20 | Bút viết kính | Cái | 0,020 |
| 21 | Bút bi | Cái | 0,010 |
| 22 | Bật lửa | Cái | 0,010 |
| 23 | Sổ lưu kết quả xét nghiệm | Tờ | 0,001 |
| 24 | Cồn sát trùng tay nhanh | ml | 2,000 |
| 25 | Dung dịch nước rửa tay | ml | 8,000 |
| 26 | Khăn lau tay | Cái | 0,030 |
| 27 | Giấy trả kết quả xét nghiệm | Tờ | 2,000 |
5. Bệnh phẩm
Vẩy da.
6. Phiếu xét nghiệm
Điền đầy đủ thông tin theo mẫu yêu cầu
III. CÁC BƯỚC TIẾN HÀNH
- Dùng kính lúp soi vùng lông và da mu, chú ý vùng chân lông tìm rận mu, thân lông để tìm ấu trùng hoặc trứng. Sau đó, dùng lược mau chải từ chân lông ra ngọn một cách nhẹ nhàng và hứng vào 1 tờ giấy trắng.
- Có thể dùng dao cùn cạo vùng lông và da mu, hứng vào lam kính
– Nhỏ 1 giọt KOH 20%, hoặc dầu Parafin, đậy lamen, soi ngay dưới kính hiển vi quang học.
Thực hiên xét nghiêm trong 5 phút và đọc kết quả sau 10 phút
IV. NHẬN ĐỊNH KẾT QUẢ
Dùng vật kính 10X để quan sát
- Rận mu:
+ Cơ thể chia làm 3 phần rõ rệt: Đầu có vòi, ăng ten, mắt đơn, ngực có 3 đốt, bụng có 9 đốt.
+ Rận trưởng thành có 3 cặp chân, ấu trùng có 4 cặp chân đối xứng nhau.
- Ngoài ra, trên tiêu bản có thể thấy trứng rận bám trên thân lông.
V. NHỮNG SAI SÓT VÀ XỬ TRÍ
1. Sai sót
- Lấy bệnh phẩm tại thương tổn không điển hình
- Bệnh phẩm quá dầy hoặc quá mỏng
- Phân biệt với Rận gây bệnh ở súc vật: Rận, Ghẻ chó, mèo…
- Người bệnh bôi thuốc diệt ký sinh trùng
2. Xử trí
- Chọn thương tổn điển hình (như mô tả)
- Dùng ngón trỏ dàn mỏng bệnh phẩm
- Nhận định hình thái điển hình ký sinh trùng rận (như mô tả trên)
- Người bệnh không bôi thuốc diệt ký sinh trùng trước đó 3-5 ngày.
Sarcoptes scabies hominis (Ghẻ) soi tươi
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đích
Phát hiện hình thái ký sinh trùng ghẻ gây bệnh ngoài da
2. Nguyên lý
Dưới tác dụng của KOH 10% biểu mô sừng mềm và mỏng do đó bộc lộ hình thái ghẻ.
II. CHUẨN BỊ
1. Người thực hiện
- Người thực hiện : Cán bộ xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành Vi sinh – Ký sinh trùng.
- Người nhận định và phê duyệt kết quả: Cán bộ có trình độ đại học hoặc sau đại học về chuyên ngành Vi sinh – Ký sinh trùng.
2. Phương tiện, hóa chất
Phương tiện, hóa chất như ví dụ dưới đây hoặc tương đương.
Trang thiết bị
- Kính hiển vi quang học
- Dụng cụ sấy lam (nếu có)
Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
| STT | Chi phí hóa chất, vật tư tiêu hao | Đơn vị | Số lượng |
| 1 | Lá kính | Cái | 1,000 |
| 2 | Lam kính | Cái | 2,000 |
| 3 | Lam kính (kiểm chuẩn) | Cái | 0,200 |
| 4 | Dung dịch KOH 10% | Ml | 1,000 |
| 5 | Dao cùn | Cái | 2,000 |
| 6 | Bông | Kg | 0,001 |
| 7 | Cồn 90 độ (vệ sinh dụng cụ) | Ml | 10,000 |
| 8 | Đèn cồn | Cái | 0,0001 |
| 9 | Panh | Cái | 0,0001 |
| 10 | Khay đựng bệnh phẩm | Cái | 0,0001 |
| 11 | Hộp vận chuyển bệnh phẩm | Cái | 0,0001 |
| 12 | Mũ | Cái | 0,020 |
| 13 | Khẩu trang | Cái | 0,020 |
| 14 | Găng tay | Đôi | 3,000 |
| 15 | Găng tay xử lý dụng cụ | Đôi | 0,020 |
| 15 | Quần áo bảo hộ | Bộ | 0,001 |
| 16 | Ống nghiệm thủy tinh | Ống | 1,000 |
| 17 | Bút viết kính | Cái | 0,020 |
| 18 | Bút bi | Cái | 0,010 |
| 19 | Bật lửa | Cái | 0,010 |
| 20 | Sổ lưu kết quả xét nghiệm | Tờ | 0,001 |
| 21 | Cồn sát trùng tay nhanh | ml | 2,000 |
| 22 | Dung dịch nước rửa tay | ml | 8,000 |
| 23 | Khăn lau tay | Cái | 0,030 |
| 24 | Giấy trả kết quả xét nghiệm | Tờ | 2,000 |
QC ký sinh trùng Demodex: Có bộ tiêu bản mẫu
3.Bệnh phẩm
Vẩy da.
4.Phiếu xét nghiệm
Điền đầy đủ thông tin theo mẫu yêu cầu
III. CÁC BƯỚC TIẾN HÀNH
1.Lấy bệnh phẩm
Theo đúng quy định của chuyên ngành Vi sinh.
2.Tiến hành kỹ thuật
- Xác định luống ghẻ
- Làm test BI
- Nhỏ dung dịch KOH 10%, đậy lamen xem dưới kính hiển vi. Thực hiên kỹ thuật trong 5 phút và nhận định kết quả trong 10 phút.
IV. NHẬN ĐỊNH KẾT QUẢ
Cái ghẻ:
+ Hình thái: Cơ thể chia làm 3 phần rõ rệt. Hình dạng bầu dục, màu trắng xám, miệng ngắn lưng gồ.
+ Con trưởng thành có 4 cặp chân, ấu trùng có 3 cặp chân đối xứng nhau
+ Ngoài ra, thấy các thành phần khác như: Trứng, ấu trùng hoặc chất thải của Ghẻ.
V. NHỮNG SAI SÓT VÀ XỬ TRÍ
1. Sai sót
- Lấy bệnh phẩm tại thương tổn không điển hình
- Bệnh phẩm nhiều vẩy da
- Bệnh phẩm quá dầy hoặc quá mỏng
- Phân biệt với ghẻ gây bệnh ở súc vật: ghẻ chó, mèo…
- Người bệnh bôi thuốc diệt ký sinh trùng
2. Xử trí
- Chọn thương tổn điển hình (như mô tả)
- Dùng ngón trỏ dàn mỏng bệnh phẩm
- Nhận định hình thái điển hình ký sinh trùng ghẻ (như mô tả trên)
- Người bệnh không bôi thuốc diệt ký sinh trùng trước đó 3-5 ngày.
Sarcoptes scabies hominis (Ghẻ) nhuộm soi
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đích
Phát hiện hình thái ghẻ gây bệnh ngoài da
2. Nguyên lý
Dưới tác dụng của glycerin hoăc dầu thực vật bộc lộ hình thái ghẻ
II. CHUẨN BỊ
1. Người thực hiện
- Người thực hiện: Cán bộ xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành Vi sinh – Ký sinh trùng.
- Người nhận định và phê duyệt kết quả: Cán bộ có trình độ đại học hoặc sau đại học về chuyên ngành Vi sinh – Ký sinh trùng.
2. Phương tiện, hóa chất
Phương tiện, hóa chất như ví dụ dưới đây hoặc tương đương.
Trang thiết bị
- Kính hiển vi quang học
- Bàn lấy bệnh phẩm
- Hộp đựng dao cùn đã tiệt trùng
- Giá đựng lam
- Kính núp
Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
| STT | Chi phí hóa chất, vật tư tiêu hao | Đơn vị | Số lượng |
| 1 | Dao cùn đã tiệt trùng | Cái | 1,000 |
| 2 | Dầu thực vật | Ml | 2,000 |
| 3 | Lam kính, lá kính | Cái | 1,000 |
| 4 | Găng tay | Đôi | 1,000 |
| 5 | Bút viết kính | Cái | 1,000 |
| 6. | Dung dịch Xanhmetylen | Ml | 2,000 |
3.Bệnh phẩm
Vẩy da
4.Phiếu xét nghiệm
Điền đầy đủ thông tin theo mẫu phiếu yêu cầu
III. CÁC BƯỚC TIẾN HÀNH
1.Lấy bệnh phẩm
- Cạo vẩy da bằng dao cùn
- Xác định luống ghẻ:
+ Là đường chỉ nhỏ ngoằn nghoèo dài từ 3 đến 10 mm
+ Có màu xám hoặc đen
+ Cuối luống ghẻ là điểm phình to
+ Lấy dao cùn cạo sâu vào da có thể bắt được cái ghẻ
- Ngoài ra nên lấy nhiều vị trí khác:
+ Kẽ tay
+ Nếp lằn vú
+ Vùng bẹn
+ Mông
+ Quy đầu
2. Tiến hành kỹ thuật
Làm test Burown ink
- Nhỏ 2-3 giọt Xanhmetylen vào điểm đầu đường hầm (rãnh ghẻ)
- Giữ yên trong thời gian 10 – 15 phút
- Sau đó đem soi ngay dưới ánh đèn
Dùng dao cùn cạo vào điểm phình to cuối luống ghẻ
Phết lên lam đã nhỏ sẵn 1 giọt dầu thực vật
Đậy lamen, soi dưới kính hiển vi quang học.
Thực hiện kỹ thuật trong 10 phút và đọc kết quả sau 5 – 10 phút
IV. NHẬN ĐỊNH KẾT QUẢ
Dùng vật kính 10X để xác định:
– Cái ghẻ
+ Hình thể: Cơ thể không chia làm 3 phần rõ rệt. Hình dạng bầu dục, màu trắng xám, miệng ngắn, lưng gồ và không có mắt, đầu có vòi hút thức ăn, đồng thời đào hầm vào thượng bì.
+ Con trưởng thành có 4 cặp chân, ấu trùng có 3 cặp chân, đối xứng
nhau.
+ Kích thước: Cái ghẻ: 330 – 250mm. Ghẻ đực : 220 – 150mm
- Trong dầu thực vật cái ghẻ di động được dễ dàng
- Ngoài ra, ta còn thấy các thành phần khác của ghẻ như: Trứng, ấu trùng hoặc chất thải của ghẻ.
V. NHỮNG SAI SÓT VÀ XỬ TRÍ
1. Sai sót
- Bệnh phẩm nhiều vẩy da nên khó nhận định khi soi trong dầu hay
- Lấy thương tổn không điển hình và ít vị trí
- Phân biệt với các loại Ghẻ khác gây bệnh cho súc vật như: Ghẻ chó, mèo
- Người bệnh bôi thuốc diệt ký sinh trùng.
2. Xử trí
- Đối với Ghẻ tăng sừng (Ghẻ Na-uy) có thể cạo bỏ lớp vẩy da, sau đó dùng kính lúp soi vào vùng thương tổn để cạo vẩy và đôi khi có thể thấy rất nhiều cái ghẻ.
- Chọn thương tổn điển hình và lấy nhiều vị trí. Mỗi vị trí một lam
- Khi tìm thấy được cái ghẻ với đặc điểm mô tả như trên là tiêu chuẩn vàng để chẩn đoán xác định. Ngoài ra, trên tiêu bản có thể thấy ấu trùng, trứng, phân hoặc một trong các loại trên.
- Người bệnh bôi thuốc diệt ký sinh trùng phải ngừng từ 3-5 ngày.
Vi nấm soi tươi
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đích
Nhận định sơ bộ vi nấm.
2. Nguyên lý
Nhận định sơ bộ vi nấm dựa vào hình thể, kích thước, cấu tạo và tính chất bắt màu.
II. CHUẨN BỊ
1.Người thực hiện
- Người thực hiện: Cán bộ xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành Vi sinh – Ký sinh trùng.
- Người nhận định và phê duyệt kết quả: Cán bộ có trình độ đại học hoặc sau đại học về chuyên ngành Vi sinh – Ký sinh trùng
2. Phương tiện, hóa chất
Phương tiện, hóa chất như ví dụ dưới đây hoặc tương đương.
Trang thiết bị
- Kính hiển
- Tủ an toàn sinh học cấp 2
- Máy li tâm
Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
| STT | Chi phí hóa chất, vật tư tiêu hao | Đơn vị | Số lượng |
| 1 | Lọ lấy bệnh phẩm | Lọ | 1,000 |
| 2 | Lam kính | Cái | 2,000 |
| 3 | Lá kính | Cái | 2,000 |
| 4 | Bông | Kg | 0,001 |
| 5 | Cồn 90 độ (vệ sinh dụng cụ) | ml | 10,000 |
| 6 | Panh | Cái | 0,0001 |
| 7 | Khay đựng bệnh phẩm | Cái | 0,0001 |
| 8 | Hộp vận chuyển bệnh phẩm | Cái | 0,0001 |
| 9 | Hóa chất (KOH, mực tàu, nước muối sinh lý) | ml | 5,000 |
| 10 | Pipet nhựa | Cái | 2,000 |
| 11 | Axit ngâm lam | ml | 10,000 |
| 12 | Ống nghiệm thủy tinh | Ống | 1,000 |
| 13 | Mũ | Cái | 0,020 |
| 14 | Khẩu trang | Cái | 0,020 |
| 15 | Găng tay | Đôi | 3,000 |
| 16 | Găng tay xử lý dụng cụ | Đôi | 0,020 |
| 17 | Quần áo bảo hộ | Bộ | 0,001 |
| 18 | Bút viết kính | Cái | 0,020 |
| 19 | Bút bi | Cái | 0,010 |
| 20 | Bật lửa | Cái | 0,010 |
| 21 | Sổ lưu kết quả xét nghiệm | Quyển | 0,001 |
| 22 | Cồn sát trùng tay nhanh | ml | 1,000 |
| 23 | Dung dịch nước rửa tay | ml | 8,000 |
| 24 | Khăn lau tay | Cái | 0,010 |
| 25 | Giấy trả kết quả xét nghiệm | Tờ | 2,000 |
| 26 | QC (nếu thực hiện) * | 0,1 | |
| 27 | EQAS (nếu thực hiện) * | 0,005 |
Ghi chú:
-
- Chi phí nội kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình nội kiểm (QC) là 1/10 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lượng ≥ 10 mẫu cho 1 lần tiến hành kỹ thuật).
- Chi phí ngoại kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình ngoại kiểm (EQAS) là 1/200 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lần ngoại kiểm trung bình 2 lần/1 năm).
3.Bệnh phẩm
Máu, dịch, mủ, đờm, phân, nước tiểu, da, tóc, móng.
4.Phiếu xét nghiệm
Điền đầy đủ thông tin theo mẫu phiếu yêu cầu
III. CÁC BƯỚC TIẾN HÀNH
1.Lấy bệnh phẩm
Theo đúng quy định của chuyên ngành Vi sinh( xem Phụ lục 5).
2.Tiến hành kỹ thuật
- Lấy bệnh phẩm cho lên lam kính: tùy từng loại bệnh phẩm sử dụng hóa chất khác
- Bệnh phẩm da, tóc, móng: Lấy bệnh phẩm lên lam kính, nhỏ dung dịch KOH 20% lên trên bệnh phẩm.
- Bệnh phẩm dịch tiết( lấy bằng que tăm bông), phân, đờm: Nhỏ NaCl 9‰ lên trên lam kính, lấy bệnh phẩm hòa lên trên giọt dung dịch đến khi đục.
- Bệnh phẩm là dịch não tủy nghi ngờ nhiễm Cryptococcus spp làm tiêu bản bằng mực tàu.
- Đối với bệnh phẩm là các chất dịch lỏng lấy trực tiếp bệnh phẩm lên lam kính.
Lấy lá kính đậy lên trên giọt dung dịch.
Quan sát kính hiển vi vật kính 10X – 40X.
IV. NHẬN ĐỊNH KẾT QUẢ
1. Dương tính
- Tế bào nấm men hình tròn hoặc bầu dục kích thước 3- 5µm nảy chồi hoặc không.
- Tế bào nấm men có quầng sáng bao quanh khi làm tiêu bản mực tàu.
- Sợi nấm giả (Sợi nhánh được tạo thành từ các chỗ thắt).
- Nấm sợi có vách ngăn (sợi nhánh được tách ra cách vách ngăn).
2. Âm tính
Không thấy vi nấm.
V. NHỮNG SAI SÓT VÀ XỬ TRÍ
- Đối với bệnh phẩm da, tóc, móng để thời gian ngắn chưa tan hết phải để thêm thời
- Tiêu bản mực tàu làm quá đen phải pha thêm nước muối sinh lý.
Vi nấm test nhanh
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đích
Phát hiện vi nấm
2. Nguyên lý
Phát hiện kháng nguyên vi nấm qua phản ứng kết hợp đặc hiệu của kháng nguyên và kháng thể tương ứng.
II. CHUẨN BỊ
1.Người thực hiện
- Người thực hiện: Cán bộ xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành Vi sinh – Ký sinh trùng.
- Người nhận định và phê duyệt kết quả: Cán bộ có trình độ đại học hoặc sau đại học về chuyên ngành Vi sinh – Ký sinh trùng
2. Phương tiện, hóa chất
Phương tiện, hóa chất như ví dụ dưới đây hoặc tương đương.
Trang thiết bị
- Tủ an toàn sinh học 2
- Micropipette
- Đồng hồ bấm giây
- Máy ly tâm thường
Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
| STT | Chi phí hóa chất, vật tư tiêu hao | Đơn vị | Số lượng |
| 1 | Ống lấy bệnh phẩm | Ống | 1,000 |
| 2 | Bơm tiêm | Cái | 1,000 |
| 3 | Bông | Kg | 0,001 |
| 4 | Cồn 90 độ (vệ sinh dụng cụ) | Ml | 10,000 |
| 5 | Panh | Cái | 0,0001 |
| 6 | Khay đựng bệnh phẩm | Cái | 0,0001 |
| 7 | Hộp vận chuyển bệnh phẩm | Cái | 0,0001 |
| 8 | Hóa chất chính | Test | 1,000 |
| 9 | Khấu hao sinh phẩm cho chạy chứng và kiểm tra chất lượng | Test | 0,400 |
| 10 | Đầu côn vàng | Cái | 2,000 |
| 11 | Axit ngâm rửa | Ml | 10,000 |
| 12 | Ống nghiệm thủy tinh | Ống | 1,000 |
| 13 | Mũ | Cái | 0,020 |
| 14 | Khẩu trang | Cái | 0,020 |
| 15 | Găng tay | Đôi | 2,000 |
| 16 | Găng tay xử lý dụng cụ | Đôi | 0,020 |
| 17 | Quần áo bảo hộ | Bộ | 0,001 |
| 18 | Bút viết kính | Cái | 0,020 |
| 19 | Bút bi | Cái | 0,010 |
| 20 | Sổ lưu kết quả xét nghiệm | Quyển | 0,001 |
| 21 | Cồn sát trùng tay nhanh | Ml | 1,000 |
| 22 | Dung dịch nước rửa tay | Ml | 8,000 |
| 23 | Khăn lau tay | Cái | 0,010 |
| 24 | Giấy trả kết quả xét nghiệm | Tờ | 2,000 |
3. Bệnh phẩm
Dịch não tủy, huyết thanh hoặc huyết tương của người bệnh
4. Phiếu xét nghiệm
Điền đầy đủ thông tin theo mẫu phiếu yêu cầu
III. CÁC BƯỚC TIẾN HÀNH
1.Lấy bệnh phẩm
Theo đúng quy định của chuyên ngành Vi sinh ( xem Phụ lục 5).
2. Tiến hành kỹ thuật
- Ly tâm ống bệnh phẩm (nếu bệnh phẩm là máu)
- Nhỏ dung dịch pha loãng vào tube sạch
- Nhỏ bệnh phẩm vào tube có dung dịch pha loãng, ghi mã bệnh phẩm tương ứng
- Cắm thanh xét nghiệm vào tube, đọc kết quả đúng thời gian qui định
IV. NHẬN ĐỊNH KẾT QUẢ
Kết quả được chấp nhận khi xuất hiện màu rõ ràng, sắc nét ở vạch chứng C
+ Dương tính khi xuất hiện màu ở vạch C và vạch T
+ Âm tính khi xuất hiện màu ở vạch chứng C và không xuất hiện màu ở vạch T.
+ Không có giá trị: Vạch chứng C không xuất hiện sau thời gian qui định thì cần kiểm tra lại hóa chất, các bước thực hiện, làm lại test khác.
V. NHỮNG SAI SÓT VÀ XỬ TRÍ
- Đọc kết quả trước hoặc sau thời gian qui định có thể làm sai lệch kết quả.
- Cho quá ít bệnh phẩm, hay quá nhiều dung dịch pha loãng có thể ảnh hưởng đến nhận định kết quả.
- Tham khảo thêm hướng dẫn của nhà sản xuất.
Vi nấm nhuộm soi
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đich
Phát hiện Pneumocystis jirovecii
2. Nguyên lý
Pneumocystis jirovecii được phát hiện nhờ hình thể, kích thước, tính chất bắt màu khi nhuộm TBO ( Toludine Blue O).
II. CHUẨN BỊ
1.Người thực hiện
- Người thực hiện: Cán bộ xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành Vi sinh – Ký sinh trùng.
- Người nhận định và phê duyệt kết quả: Cán bộ có trình độ đại học hoặc sau đại học về chuyên ngành Vi sinh – Ký sinh trùng
2. Phương tiện, hóa chất
Trang thiết bị
Kính hiển vi quang học Tủ an toàn sinh học cấp 2 Máy ly tâm
Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
| STT | Chi phí hóa chất, vật tư tiêu hao | Đơn vị | Số lượng |
| 1 | Lọ lấy bệnh phẩm | Lọ | 1,000 |
| 2 | Que lấy bệnh phẩm | Cái | 2,000 |
| 3 | Lam kính | Cái | 1,000 |
| 5 | Bông | Kg | 0,001 |
| 6 | Cồn 90 độ (vệ sinh dụng cụ) | ml | 10,000 |
| 7 | Panh | Cái | 0,0001 |
| 8 | Khay đựng bệnh phẩm | Cái | 0,0001 |
| 9 | Hộp vận chuyển bệnh phẩm | Cái | 0,0001 |
| 10 | Dung dịch TBO | ml | 3,000 |
| 11 | Pipet nhựa | Cái | 2,000 |
| 12 | Axit ngâm lam | ml | 10,000 |
| 13 | Ống nghiệm thủy tinh | Ống | 1,000 |
| 14 | Mũ | Cái | 0,020 |
| 15 | Khẩu trang | Cái | 0,020 |
| 16 | Găng tay | Đôi | 3,000 |
| 17 | Găng tay xử lý dụng cụ | Đôi | 0,020 |
| 18 | Quần áo bảo hộ | Bộ | 0,001 |
| 19 | Bút viết kính | Cái | 0,020 |
| 20 | Bút bi | Cái | 0,010 |
| 21 | Bật lửa | Cái | 0,010 |
| 22 | Sổ lưu kết quả xét nghiệm | Quyển | 0,001 |
| 23 | Cồn sát trùng tay nhanh | ml | 1,000 |
| 24 | Dung dịch nước rửa tay | ml | 8,000 |
| 25 | Khăn lau tay | Cái | 0,010 |
| 26 | Giấy trả kết quả xét nghiệm | Tờ | 2,000 |
| 27 | QC (nếu thực hiện) * | 0,1 | |
| 28 | EQAS (nếu thực hiện) * | 0,005 |
* Ghi chú:
- Chi phí nội kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình nội kiểm (QC) là 1/10 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lượng ≥ 10 mẫu cho 1 lần tiến hành kỹ thuật).
- Chi phí ngoại kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình ngoại kiểm (EQAS) là 1/200 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lần ngoại kiểm trung bình 2 lần/1 năm).
3.Bệnh phẩm
Đờm, dịch phế quản.
4.Phiếu xét nghiệm
Điền đầy đủ thông tin theo mẫu phiếu yêu cầu
III. Các bước tiến hành
1.Lấy bệnh phẩm
Theo đúng quy định của chuyên ngành Vi sinh ( xem Phụ lục 5).
2. Tiến hành kỹ thuật
- Lấy bệnh phẩm phết lên lam kính, để khô.
- Phủ thuốc nhuộm TBO lên trên bệnh bệnh phẩm.
- Rửa nước, để khô.
- Quan sát kính hiển vi vật kính 40X-
IV. NHẬN ĐỊNH KẾT QUẢ
1. Dương tính
- Thể hoạt động Pneumocystis jirovecii kích thước từ 1- 4µm.
- Thể bào nang bắt màu xanh tím hình tròn vỏ mỏng kích thước 1- 7µm bên trong có từ 1-8 nhân.
2. Âm tính
Không tìm thấy Pneumocystis jirovecii.
V. NHỮNG SAI SÓT VÀ XỬ TRÍ
- Tiêu bản bị bong .
- Xử trí
- Khi phết lam phải để bệnh phẩm khô mới tiến hành nhuộm.